
关于氧化还原反应,下列说法正确的是( )
①Mg在化学反应中失去2个电子,而Al在化学反应中失去3个电子 ,因此还原性Al>Mg;
②氧化剂具有氧化性;
③有单质参加的反应一定是氧化还原反应;
④2Fe+3Cl2 2FeCl3;Fe+S
2FeCl3;Fe+S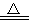 FeS,由此可以判断氧化性:Cl
FeS,由此可以判断氧化性:Cl 2>S
2>S
⑤氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
A.②③④ B.②④ C.①②⑤ D.①②
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源:2016-2017学年西藏山南二中高二上学期期中化学试卷(解析版) 题型:选择题
对于可逆反应A(g)+ 2B(g) 2C(g)(正反应吸热),下列图象中正确的是( )
2C(g)(正反应吸热),下列图象中正确的是( )
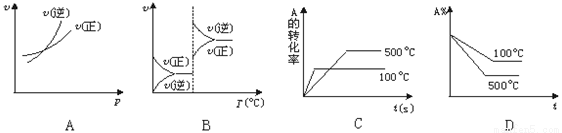
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省等六校高一上期中化学卷(解析版) 题型:选择题
实验室里需用480mL 0.1mol•L﹣1的碳酸钠溶液,选取500mL容量瓶进行配制,以下操作正确的是
A. 称取5.1gNa2CO3,加入500mL水
B. 称取13.7gNa2CO3·10H2O,配成500mL溶液
C. 称取5.3Na2CO3,加入500mL水
D. 称取14.3gNa2CO3·10H2O,配成500mL溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高一上期中化学卷(解析版) 题型:推断题
碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是: 在溶液中 KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)用双线桥表示该反应中电子转移的方向和数目:___________________
当有0.2molKIO3与足量的KI反应时氧化剂与还原剂的物质的量之比是___ _____,转移的电子数目为 _ _ ___
(2)实验结束后分离I2和K2SO4溶液所用的方法是 ,所用的分离试剂是 ,所用的玻璃仪器有 .
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制0.5mol/L的稀硫酸溶液450mL,需量取98%的浓硫酸(其密度为1.84g/cm3)的体积为 ml,配制中需要用到的主要玻璃仪器有烧杯、玻璃棒、胶头滴管 .
(4)下面操作造成所配稀硫酸溶液浓度偏小的是_____________(填序号)
A.溶解的时候溶液没有冷却到室温就转移 |
B.转移时没有洗涤烧杯、玻璃棒 |
C.向容量瓶加水定容时眼睛俯视液面 |
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶 |
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高一上期中化学卷(解析版) 题型:选择题
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序( )
①过滤;②加过量NaOH溶液;③加适量盐酸; ④加过量Na2CO3溶液;⑤加过量BaCl2溶液.
A.②⑤④①③ B.⑤④②③① C.④②⑤①③ D.④①②⑤③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省赣州市十四校高一上期中化学卷(解析版) 题型:选择题
①氯化钠溶液和鸡蛋清 ②氯化钠溶液中少量的硝酸钾 ③碳酸钡和氯化钡的溶液分离以上三组混合物依次采取的方法正确的是( )
A .渗析、结晶、过滤 B.渗析、蒸馏、过滤
C .蒸馏、萃取、分液 D.分液、过滤、加热升华
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省蕲春县高一上学期期中化学试卷(解析版) 题型:选择题
如图是高温下某反应的微观过程.下列说法中正确的是
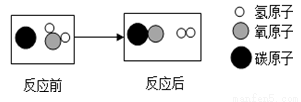
A.该反应属于分解反应
B.图中的两种化合物都属于氧化物
C.该反应中元素的化合价没有变化
D.反应前后原子的种类改变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省蕲春县高二上学期期中化学试卷(解析版) 题型:实验题
实验室以一种工业废渣(主要成分为MgCO3、MgSO4和少量Fe、Al的氧化物)为原料制备MgCO3?3H2O。实验过程如下:

(1)酸溶需加热的目的是 ;过滤时用到的玻璃仪器有 ;
(2)加入H2O2氧化时发生发应的离子方程式为 。
(3)用如图所示的实验装置进行萃取和分液,以除去溶液中的Fe3+。
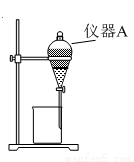
①实验装置图中仪器A的名称为 。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有溶液的仪器A中加入一定量的有机萃取剂, 、静置、分液,并重复多次。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高二上学期期中化学试卷(解析版) 题型:填空题
830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g) CO2(g)+H2(g)△H>0
CO2(g)+H2(g)△H>0
试回答下列问题:
(1)请写出该化学反应的平衡常数表达式:___________。
(2)830K温度下,若起始时c(CO)=2mol·L-1,c(H2O)=3mol·L-1,达到平衡时CO的转化率为50%,则在该温度下,该反应的平衡常数K=______________
(3)若降低温度,该反应的K值将________,该反应的正反应速率将___________;该反应的逆反应速率将__________(均填“增大”“减小”或“不变”)。
(4)若要提高CO的转化率,可采取的措施有:___________。
(5)830K温度下,若起始时c(CO)=1mol·L-1,c(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5mol·L-1,则此时该反应是否达到平衡状态___________(填“是”与“否”),你判断的依据是:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com