
 ijŹµŃ銔×éĶ¬Ń§ĪŖĮĖĢ½¾æĶÓėÅØĮņĖįµÄ·“Ó¦£¬½ųŠŠČēĻĀŹµŃ锣
ijŹµŃ銔×éĶ¬Ń§ĪŖĮĖĢ½¾æĶÓėÅØĮņĖįµÄ·“Ó¦£¬½ųŠŠČēĻĀŹµŃ锣
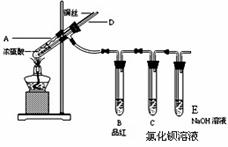
ŹµŃé1£ŗĶÓėÅØĮņĖį·“Ó¦£¬ŹµŃé×°ÖĆČēĶ¼ĖłŹ¾”£
ŹµŃé²½Öč£ŗ
¢ŁĻČĮ¬½ÓŗĆ×°ÖĆ£¬¼ģŃéĘųĆÜŠŌ£¬¼ÓČėŹŌ¼Į£»
¢Ś¼ÓČČAŹŌ¹ÜÖ±µ½BÖŠĘ·ŗģĶŹÉ«£¬ĻØĆš¾Ę¾«µĘ£»
¢Ū½«CuĖæÉĻĢįĄėæŖŅŗĆę£»
£Ø1£©Äܹ»Ö¤Ć÷ĶÓėÅØĮņĖį·“Ó¦²śÉśµÄĘųĢåµÄĻÖĻó£ŗ ”£
£Ø2£©ŌŚŹ¢ÓŠĀČ»Æ±µČÜŅŗµÄCŹŌ¹ÜÖŠ³żĮĖµ¼¹ÜæŚÓŠĘųÅŻĶā£¬ĪŽĘäĖūĆ÷ĻŌĻÖĻó£¬Čō½«Ęä·ÖĪŖĮ½·Ż£¬·Ö±šµĪ¼ÓĻĀĮŠČÜŅŗ£¬½«²śÉś³ĮµķµÄ»ÆѧŹ½ĢīČėĻĀ±ķĻąÓ¦Ī»ÖĆ”£
| µĪ¼ÓµÄČÜŅŗ | ĀČĖ® | °±Ė® |
| ³ĮµķµÄ»ÆѧŹ½ | __________________________ | __________________________ |
Š“³öĘäÖŠSO2ĻŌŹ¾»¹ŌŠŌµÄĄė×Ó·½³ĢŹ½£ŗ ”£
£Ø3£©ĻØĆš¾Ę¾«µĘŗó£¬ŅņĪŖÓŠµ¼¹ÜDµÄ“ęŌŚ£¬BÖŠµÄŅŗĢå²»»įµ¹Īü£¬
ĘäŌŅņŹĒ: ”£
£Ø4£©½«SO2ĘųĢåĶØČėŗ¬ÓŠn mol Na2SČÜŅŗÖŠ£¬ČÜŅŗÖŠ³öĻÖ»ĘÉ«»ė×Ē£¬ŹŌ·ÖĪöøĆČÜŅŗ×ī¶ąÄÜĪüŹÕSO2ĘųĢå mol”£ £Ø²»æ¼ĀĒČܽāµÄSO2£©”£
 Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø
Ģį·Ö°Ł·Ö°Ł¼ģ²ā¾ķĻµĮŠ“š°ø ±¦±“¼Ę»®ĘŚÄ©³å“Ģ¶į100·ÖĻµĮŠ“š°ø
±¦±“¼Ę»®ĘŚÄ©³å“Ģ¶į100·ÖĻµĮŠ“š°ø ÄÜæ¼ŹŌČ«ÄÜ100·ÖĻµĮŠ“š°ø
ÄÜæ¼ŹŌČ«ÄÜ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠ¹ŲŗĻ³É°±¹¤ŅµµÄĻĀĮŠĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ(””””)
A£®“ÓŗĻ³ÉĖž³öĄ“µÄ»ģŗĻĘųĢ壬NH3µÄŗ¬Įæ½ĻŠ”£¬ĖłŅŌÉś²ś°±µÄ¹¤³§µÄŠ§ĀŹ¶¼ŗܵĶ
B£®ÓÉÓŚ°±æÉŅŗ»Æ·ÖĄė³öĄ“£¬N2”¢H2ŌŚŹµ¼ŹÉś²śÖŠŃ»·Ź¹ÓĆ£¬ĖłŅŌ×ÜĢåĄ“Ėµ°±µÄ²śĀŹŗÜøß
C£®ŗĻ³É°±¹¤ŅµµÄ·“Ó¦ĪĀ¶ČæŲÖĘŌŚ500 ”ę£¬ÄæµÄŹĒŹ¹»ÆŃ§Ę½ŗāĻņÕż·“Ó¦·½ĻņŅʶÆ
D£®ŗĻ³É°±³§²ÉÓƵÄŃ¹ĒæŹĒ20 MPa”«50 MPa£¬ŅņŌŚøĆŃ¹ĒæĻĀĢś“„Ć½µÄ»īŠŌ×ī“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠŅŌĻĀĪļÖŹ£ŗ
¢ŁNaCl¹ĢĢå ¢ŚŃĪĖį ¢ŪBa(OH)2ČÜŅŗ ¢ÜĶ ¢Ż¶žŃõ»ÆĢ¼ĘųĢå ¢ŽĮņĖįĒā¼Ų¹ĢĢå
¢ßŅŅ“¼(C2H5OH) ¢ąŅŗĢ¬ĮņĖį ¢įČŪČŚĢ¬BaSO4 ¢āŅŗĢ¬SO3
Ēė»Ų“šĻĀĮŠĪŹĢā(ÓĆŠņŗÅ)£ŗ
ŅŌÉĻĪļÖŹÖŠŹōÓŚ»ÆŗĻĪļµÄŹĒ”” £ØĢīŠņŗÅ£¬ĻĀĶ¬£©£¬ŹōÓŚŃĪµÄŹĒ”” ”” £¬ŹōÓŚŃõ»ÆĪļµÄŹĒ , Äܵ¼µēµÄŹĒ_______________________£¬ŹōÓŚµē½āÖŹµÄŹĒ______________________£¬ŹōÓŚ·Ēµē½āÖŹµÄŹĒ___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĻĀĮŠŹµŃ飬ŹµŃé½į¹ūÓėŌ¤²āµÄĻÖĻó²»Ņ»ÖĀµÄŹĒ£Ø £©
| ¢ŁÖŠµÄĪļÖŹ | ¢ŚÖŠµÄĪļÖŹ | Ō¤²ā¢ŁµÄĻÖĻó |
| |
| A | µķ·ŪKIČÜŅŗ | ÅØĻõĖį | ĪŽĆ÷ĻŌ±ä»Æ | |
| B | ·ÓĢŖČÜŅŗ | ÅØŃĪĖį | ĪŽĆ÷ĻŌ±ä»Æ | |
| C | AlCl3ČÜŅŗ | ÅØ°±Ė® | ÓŠ°×É«³Įµķ | |
| D | ŹŖČóŗģÖ½Ģõ | ±„ŗĶĀČĖ® | ŗģÖ½ĢõĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ£ŗ½«Cl2ĶØČėŹŹĮæKOHČÜŅŗ£¬²śĪļÖŠæÉÄÜÓŠKC1”¢KClO”¢KC1O3£¬ĒŅ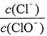
µÄÖµÓėĪĀ¶ČøßµĶÓŠ¹Ų”£µ±n(KOH)=a molŹ±£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ£Ø £©
A£®ČōijĪĀ¶ČĻĀ£¬·“Ó¦ŗó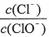 £½11£¬ŌņČÜŅŗÖŠ
£½11£¬ŌņČÜŅŗÖŠ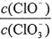 £½
£½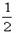
B£®²Ī¼Ó·“Ó¦µÄĀČĘųµÄĪļÖŹµÄĮæµČÓŚ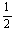 a mol
a mol
C£®øıäĪĀ¶Č£¬·“Ó¦ÖŠ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæneµÄ·¶Ī§£ŗ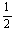 a mol”Üne”Ü
a molӆneӆ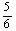 a mol
a mol
D£®øıäĪĀ¶Č£¬²śĪļÖŠKC1O3µÄ×ī“óĄķĀŪ²śĮæĪŖ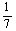 a mol
a mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijČÜŅŗÖŠµĪČėBaCl2ČÜŅŗ£¬²śÉś°×É«³Įµķ£¬ŌŁµĪČėĻ”ŃĪĖį£¬³Įµķ²»Čܽā£¬ŌņøĆČÜŅŗÖŠ
A. Ņ»¶ØÓŠSO42- B. æÉÄÜÓŠSO42- »ņAg+
C. Ņ»¶ØĪŽAg+ D. »¹æÉÄÜÓŠCO32-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ·ÖÉ¢Ļµ,²»»į²śÉś¶”“ļ¶ūŠ§Ó¦µÄŹĒ””(””””)
¢Ł¼¦µ°Ēå ¢Śµķ·ŪČÜŅŗ ¢ŪĮņĖįÄĘČÜŅŗ ¢ÜFe(OH)3½ŗĢå ¢ŻFe(OH)3Šü×ĒŅŗ
A.¢Ł¢Ū”””” B.¢Ś¢Ū¢Ż”””” C.¢Ū¢Ü¢Ż”””” D.¢Ū¢Ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
CuClŹĒÓŠ»śŗĻ³ÉµÄÖŲŅŖ“߻ƼĮ£¬²¢ÓĆÓŚŃÕĮĻ”¢·ĄøÆµČ¹¤Ņµ”£¹¤ŅµÉĻÓÉ·ĻĶĮĻ£Øŗ¬Fe”¢Al¼°Ęä»ÆŗĻĪļ”¢SiO2ŌÓÖŹ£©£¬Éś²śCuClµÄ¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ
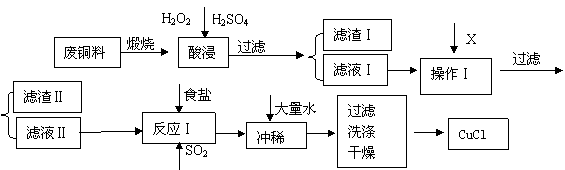
| ĪļÖŹ | æŖŹ¼³Įµķ | ³ĮµķĶźČ« |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 5.6 | 6.7 |
| Al(OH)3 | 3.8 | 4.7 |
ŅŃÖŖ£ŗCuClČÜÓŚNaClµÄÅØČÜŅŗæÉÉś³ÉCuCl2££¬CuCl2£µÄČÜŅŗÓĆĖ®Ļ”ŹĶŗóæÉÉś³ÉCuCl³Įµķ”£
£Ø1£©ģŃÉÕµÄÖ÷ŅŖÄæµÄŹĒ£ŗ ”£
£Ø2£©²Ł×÷¢ńĪŖµ÷½ŚČÜŅŗµÄPHÖµ£¬·¶Ī§ĪŖ £¬¼ÓČėµÄĪļÖŹXæÉŅŌŹĒ£Ø £©
A”¢CuO B”¢Cu(OH)2 C”¢NaOH ČÜŅŗ D”¢CaCO3
£Ø3£©ĀĖŌü¢ņµÄÖ÷ŅŖ³É·ÖŹĒ ”£
£Ø4£©ĶłĀĖŅŗ¢ņÖŠ¼ÓČėŹ³ŃĪ²¢ĶØČėSO2æÉÉś³ÉCuCl2££¬ĒėŠ“³ö·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
ӣ
£Ø5£©ŌŚ·“Ó¦¢ńÖŠ£¬ĪĀ¶ČæŲÖĘŌŚ70~80”ę²¢Ź¹ÓĆÅØNaClČÜŅŗ£¬Ö÷ŅŖÄæµÄŹĒ£ŗ ”£
£Ø6£©³£ĪĀĻĀ£¬ŅŃÖŖCuOHµÄKSPĪŖ1.0”Į10£14£¬ŌņCu++H2O  CuOH + H+µÄĘ½ŗā³£ŹżĪŖ£ŗ ”£
CuOH + H+µÄĘ½ŗā³£ŹżĪŖ£ŗ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®Ōö“ó·“Ó¦ĪļÅØ¶Č£¬æÉŌö“óµ„Ī»Ģå»żÄŚ»ī»Æ·Ö×ӵİŁ·ÖŹż£¬“Ó¶ųŹ¹ÓŠŠ§Åöײ“ĪŹżŌö“ó”£
B. ŗćČŻČŻĘ÷ÖŠĘ½ŗāĢåĻµA(g)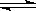 2B(g)ÖŠŌö¼ÓAµÄĪļÖŹµÄĮ棬AµÄ×Ŗ»ÆĀŹŌö“ó”£
2B(g)ÖŠŌö¼ÓAµÄĪļÖŹµÄĮ棬AµÄ×Ŗ»ÆĀŹŌö“ó”£
C. Ņ»¶ØĢõ¼žĻĀ·“Ó¦2AB(g) 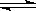 A2(g)£«B2(g), µ±ČŻĘ÷ÖŠø÷×é·ÖµÄĢå»ż·ÖŹż²»Ėꏱ¼ä±ä»Æ£¬ĖµĆ÷ĢåĻµ“ļµ½Ę½ŗāדĢ¬”£
A2(g)£«B2(g), µ±ČŻĘ÷ÖŠø÷×é·ÖµÄĢå»ż·ÖŹż²»Ėꏱ¼ä±ä»Æ£¬ĖµĆ÷ĢåĻµ“ļµ½Ę½ŗāדĢ¬”£
D. ŅŃÖŖ·“Ó¦A2£Øg£©+2B2£Øg£© 2AB2£Øg£©”÷H £¼0, ÉżøßĪĀ¶Č£¬ÕżĻņ·“Ó¦ĖŁĀŹŌö¼Ó£¬ÄęĻņ·“Ó¦ĖŁĀŹ¼õŠ””£
2AB2£Øg£©”÷H £¼0, ÉżøßĪĀ¶Č£¬ÕżĻņ·“Ó¦ĖŁĀŹŌö¼Ó£¬ÄęĻņ·“Ó¦ĖŁĀŹ¼õŠ””£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com