某物质R可用于制备高热导陶瓷基片、陶瓷刀具、切削工具,高温下材料强度大.经检测,R由两种短周期元素组成.现取123g R溶于热的KOH溶液中反应,得到无色溶液A和67.2L气体B(气体体积为标准状况下测定),该气体通入硫酸铜溶液有浅蓝色的沉淀生成,继续滴加氨水至沉淀完全溶解,此时即得深蓝色的溶液,对此溶液加热又有浅蓝色的沉淀生成.往上述过程所得无色溶液中滴加入盐酸,溶液先出现浑浊后又变澄清.
物质B与单质X及水之间相互作用,有如下转化关系:B
C
D
E.E是一种强酸,将C和D的混合物溶解在冰水中,即可得到一种弱酸F的水溶液.请回答下列问题:
(1)物质R的名称为
,属于
晶体(填“分子”、“离子”、“原子”等).B与C反应的化学方程式为:
.
(2)对深蓝色的溶液加热又有浅蓝色的沉淀生成,其原因是
(用离子方程式表示).
(3)弱酸E是一种比醋酸酸性稍强的弱酸,很不稳定,通常在室温下易分解.要制得E溶液,可以往冷冻的其钠盐浓溶液中加入或通入某种物质,下列物质不适合使用的是
(填序号).
A.二氧化碳 B.盐酸 C.二氧化硫 D.稀硫酸
(4)NO
-2是工业废水在排放前必须除去的.碱性条件下用铝粉有效除去废水中的NO
-2,已知此反应体系中检测到B气体.写出上述反应的离子方程式
.若改用电解法将废水中NO
-2转换为N
2除去,N
2将在
(填“阴极”或“阳极”)生成,电极反应为
.
(5)C1
2与B以3:1的物质的量之比反应生成HCl和一种二元化合物Y(该反应中只有一种元素化合价改变).Y大量应用于面粉的漂白和消毒,写出Y与水反应的化学方程式
.




 ,它可以发生酯化、水解、加成等反应
,它可以发生酯化、水解、加成等反应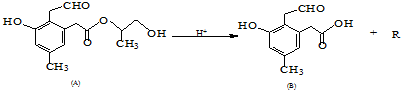
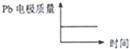
 (1)铅蓄电池是典型的二次电池,由于铅蓄电池的性能优良、价格低廉、安全可靠,可多次充放电,所以在生产生活中使用广泛,总反应式是pb+pbo2+4H++2SO42-
(1)铅蓄电池是典型的二次电池,由于铅蓄电池的性能优良、价格低廉、安全可靠,可多次充放电,所以在生产生活中使用广泛,总反应式是pb+pbo2+4H++2SO42-
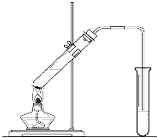 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: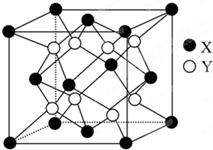 某离子晶体的晶体结构如图所示,试求:
某离子晶体的晶体结构如图所示,试求: