
如图所示,反应:X(气)+3Y(气)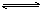 2Z(气)△H<0,在不同温度、不同压强(p1>p2)下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为
2Z(气)△H<0,在不同温度、不同压强(p1>p2)下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
按要求填空,在原子序数1—20号元素中:(共4分)
(1)与水反应最剧烈的金属是__________(填名称)。
(2)原子半径最小的元素是_____________(填符号)。
(3)气态氢化物最稳定的化学式是_____________。
(4)最高价氧化物对应水化物的酸性最强的化学式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图装置可用于收集气体X并验证其某些化学性质,你认为正确的是( )
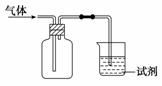
| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | SO2 | 酸性KmnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | C2H4 | 溴水 | 溶液褪色 | 能发生加成反应x k b 1 |
| C | X | 澄清石灰水 | 溶液变浑浊 | X不一定是CO2 |
| D | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知有热化学方程式:SO2(g)+ 1/2O2(g)==SO3(g) △H =-98.32kJ/mol现有5molSO2参加反应,当放出393.28kJ热量时,SO2的转化率最接近于
A.40% B.50% C.80% D.90%
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: (1)Zn(s)+1/2O2(g)==ZnO(s);ΔH=-348.3kJ/mol
(2)2Ag(s)+1/2 O2(g)== Ag2O(s);ΔH=-31.0kJ/mol
则Zn(s)+ Ag2O(s)== ZnO(s)+ 2Ag(s)的ΔH等于
A.-317.3kJ/mol B.-379.3kJ/mol
C.-332.8 kJ/mol D.+317.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
|
C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为 ,表中b c(填“<”、“=”、“>”)。
(2)20s时,N2O4的的浓度为 mol/L,0~20s内N2O4的平均反应速率为 。
(3)该反应的平衡常数表达式K= ,在80℃时该反应的平衡常数K值为 (保留2位小数)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时 。
N2O4的转化率越高
NO2的产量越大
N2O4与NO2的浓度之比越大
正反应进行的程度越大
(5)要增大该反应的K值,可采取的措施
 增大N2O4起始浓度
增大N2O4起始浓度
向混合气中通入NO2
(C) 使用高效催化剂
(D) 升高温度
(6)如图是80℃时容器中N2O4浓度的变化
图,请在该图中补画出该反应在60℃反
应时N2O4浓度的变化曲线。
查看答案和解析>>
科目:高中化学 来源: 题型:
依据元素周期表及元素周期律,下列推断正确的是
( )
A.H3BO3的酸性比H2CO3的强
B.Mg(OH)2的碱性比Be(OH)2的强
C.HCl、HBr、HI的热稳定性逐渐增强
D.若M+和R2-的核外电子层结构相同,则离子半径:M+>R2-
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.常温下,0.05 mol·L-1 Fe2(SO4)3溶液中含Fe3+数目为0.1NA
B.标准状况下,22.4 L甲苯中含C—H数目为8NA
C.常温常压下,3.2 g O2和O3混合物中,氧原子的数目为0.2NA
D.0.1 mol Na2O2与足量CO2反应时,转移的电子数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com