
����Ŀ�������������к������ߣ�����������������Ŀռ䡣�������ӵĽṹ��ͼ����V�ͣ�����116��5��������ԭ����һ��Oԭ��Ϊ���ģ�����������Oԭ�ӷֱ�һ���Ǽ��Թ��ۼ����м�Oԭ���ṩ2�����ӣ��Ա�����Oԭ�Ӹ��ṩ1�����ӣ�����һ������Ļ�ѧ����������Oԭ�Ӿ��ȵ�������4�����ӡ���ش�

�����ķ��ӽṹ
��1�������������Ĺ�ϵ��___________��
��2��ѡ�����з�����������������ڵȵ�������� ��
���������� �£��ã��� �ã��ӣ��� �ģ��£�ã���
��3��������ijԭ����1��û�и�����ԭ�ӹ��õļ۵��ӽй¶Ե��ӣ���ô����������_______ �Թ¶Ե��ӡ�
��4��������������ת���Ƿ�Ϊ������ԭ��Ӧ___________��
���𰸡� (1)ͬ�������� ��2��C ��3��5 ��4����
��������
�����������1������������������Ԫ���γɵIJ�ͬ���ʣ�����Ϊͬ�������塣
��2��ԭ�����ͼ۵������ֱ���ȵ��ǵȵ����壬��������������ڵȵ����������������ѡC��
��3�����ݳ����Ľṹ�¶Ե��ӵĺ����֪�����������к��еŶԵ�����2��1��2��5�ԡ�
��4����������������ֲ�ͬ�ĵ��ʣ�����֮���ת������ѧ�仯����û�е��ӵĵ�ʧ�����Բ���������ԭ��Ӧ��


 �����ܿ����ϵ�д�
�����ܿ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������AIST���������о�һ�������������ͳɱ����ͭ����ȼ�ϵ�ء��õ��ͨ��һ�ָ��ӵ�ͭ��ʴ���������������������зŵ����Ϊ2Li+Cu2O+H2O![]() 2Cu+2Li++2OH������˵������ȷ����
2Cu+2Li++2OH������˵������ȷ����

A. �ŵ�ʱ�������ĵ缫��ӦʽΪCu2O+H2O+2e![]() 2Cu+2OH
2Cu+2OH
B. �ŵ�ʱ��Li+������������Cu���ƶ�
C. ͨ����ʱ��ͭ����ʴ���������Cu2O
D. ������Ӧ�����У�ͭ�൱�ڴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.CO2��ת��һֱ��ȫ���о����ȵ㣬���н�CO2��H2�ϳɼ״��������� (CH3OCH3)�߱���Գ���ļ�������ҵ�����У���������ط�Ӧ
��CO2(g) + 3H2(g) ![]() CH3OH(l) + H2O(l) ��H < 0
CH3OH(l) + H2O(l) ��H < 0
��2 CH3OH(l) ![]() CH3OCH3(g) + H2O(l) ��H < 0
CH3OCH3(g) + H2O(l) ��H < 0
��CO(g) + H2O(l) ![]() CO2(g) + H2(g) ��H < 0
CO2(g) + H2(g) ��H < 0
��1����һ���º��ݵ��ܱ������У�����һ�����ļ״����ʽ����ƽ�⣬����˵����ȷ��������Ϊ�÷�Ӧ�ﵽƽ��״̬���ж�����Ϊ________��
A��������������Է����������ֲ���
B������������ѹǿ����
C����ͬʱ�������ļ״����������Ķ����ѵ�������
D���״��Ͷ��������ʵ������
��2�������������ͬ���ܱ�����A,B,C�м�����ͬ���ʵ�����CO��H2O�ڲ�ͬ�¶��·�����Ӧ�ۣ�������ͬʱ����������е�CO���ʵ������¶ȵĹ�ϵ����ͼ��

�� A��B��������ʴ�Сv(A)___v(B)������ڡ�����С�ڡ��������ڡ��������жϡ���
�� �����������CO�����ʵ����ȼ�С�������ԭ��________________________��
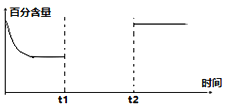
��3��һ������CO2��H2��һ�ܱ������з�����Ӧ�٣�����ͼ��������CO2�İٷֺ���������������ı�ı仯����ͼ���벹����������t1ʱ�����£�t2ʱ�̼Ӵ�����______

��.SO2��β������ͨ���õ绯ѧ������
��4����������ͼ��ʾ��Pt(��)�缫�ķ�ӦʽΪ__________________��
�ڵ���·��ת��0.02mole��ʱ(��ŨH2SO4��δ�ų�)������Ĥ�����Һ��Լ����_____mol���ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������NaOH��Һ����μ���AlCl3��Һ�����ɳ���Al��OH��3������AlCl3�������ı仯��ϵ��ͼ��ʾ���������������ڶ�Ӧ����Һ��һ���ܴ���������ǣ� ��

A. a���Ӧ����Һ�У�Na+��Fe3+��SO42����HCO3��
B. b���Ӧ����Һ�У�Na+��S2����SO42����Cl��
C. c���Ӧ����Һ�У�Ag+��Ca2+��NO3����Na+
D. d���Ӧ����Һ�У�K+��NH4+��I����HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л�����������Ũ��ʱ��ͨ����������ɱ�����������ǣ� ��
A. ������ҺB. �Ҵ���ҺC. ��ȩ��ҺD. ������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����HF��H2O��NH3��CS2��CH4��H2O2��N2�����У�������ѡ�����ʻ�ѧʽ����հף�
��1���ԷǼ��Լ���ϵķǼ��Է�����___________;
��2���Լ��Լ����ϣ�����ֱ���ͽṹ�ķǼ��Է�����___________;
��3���Լ��Լ����ϣ�������������ṹ�ķǼ��Է�����___________;
��4���Լ��Լ����ϣ����������ͽṹ�ļ��Է�����___________;
��5���Լ��Լ����ϣ�����V�ͽṹ�ļ��Է�����___________;
��6���Լ��Լ����ϣ����ҷ��Ӽ���������___________;
��7����N2O��Ϊ�ȵ��������_______________;
��8�����зǼ��Լ��ļ��Է�����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڢٱ��Ӣڼױ������������ϩ���Ҵ��У�ѡ������д��
��1���ܺͽ����Ʒ�Ӧ�ų�H2����______����2������NaOH��Һ��Ӧ����______��
��3������������Ũ��ˮ��Ӧ����__����4����ʹ����KMnO4��Һ��ɫ������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Fe2(C2O4)3��xH2Oͨ����ش����������ˮ����������ˮ������110�����ȫʧȥ�ᾧˮ��Ϊ�ⶨ�þ��������ĺ����ͽᾧˮ�ĺ�����ijʵ��С����������ʵ�飺
����1������4.66g������������д��������Ƴ�250 mLһ�����ʵ���Ũ�ȵ���Һ��
����2��ȡ������Һ25.00 mL����ƿ�У���ϡH2SO4�ữ���μ�KMnO4��Һ�������
ǡ��ȫ�������ɶ�����̼��ͬʱMnO4-����ԭ��Mn2������Ӧ�����Һ�м���һС��п�ۣ���������Һ��ɫ�պ���ʧ�����ˡ�ϴ�ӣ������˼�ϴ��������Һ�ռ�����ƿ�У���ʱ��Һ�Գ����ԡ�
����3����0.0200 mol��L-1KMnO4��Һ�ζ�����2������Һ���յ㣬����KMnO4��ҺV1 mL���ζ���MnO4-����ԭ��Mn2����
�ظ�����2������3�IJ���2�Σ��ֱ�ζ�����0.0200 mol��L-1 KMnO4��ҺΪV2��V3 mL��
��¼�������±���
ʵ���� | KMnO4��Һ��Ũ�ȣ�mol��L-1�� | KMnO4��Һ����������mL�� |
1 | 0.0200 | V1 = 20.02 |
2 | 0.0200 | V2 = 20.12 |
3 | 0.0200 | V3 = 19.98 |
��ش��������⣺
��1����������Һ������ˮ����ԭ��_________________�������ӷ���ʽ��ʾ��
��2����ʵ�鲽��1�Ͳ���3��ʹ�õ�������������ƽ������̨���ζ��ܼС��ձ����������⣬һ���������������е�______________ (�����)
��ʽ�ζ��� B����ʽ�ζ��� C����Ͳ(10 mL) D����ƿ��
E����ͷ�ι� F��©�� G��250 mL����ƿ
��3������п�۵�Ŀ����______________________
��4������3�ζ�ʱ�Ƿ�ѡ��ָʾ��_________���ǻ��˵������_________________________д������3�з�����Ӧ�����ӷ���ʽ____________________________
��5���ڲ���2�У��������KMnO4��Һ�������������õ�������________(�ƫ�͡�����ƫ�ߡ����䡱)��ʵ���øþ����нᾧˮ�ĸ���xΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ݻ�Ϊ2L���ܱ������н������·�Ӧ��A��g��+2B��g��![]() 3C��g��+XD��g������ʼʱAΪ4mol��BΪ6mol��5minĩʱ���C�����ʵ���Ϊ3mol����D��ʾ�Ļ�ѧ��Ӧ����v��D��Ϊ0.2mol/��L��min��������
3C��g��+XD��g������ʼʱAΪ4mol��BΪ6mol��5minĩʱ���C�����ʵ���Ϊ3mol����D��ʾ�Ļ�ѧ��Ӧ����v��D��Ϊ0.2mol/��L��min��������
��1��5minĩA�����ʵ���Ũ��Ϊ______________mol/L��
��2��ǰ5min����B��ʾ�Ļ�ѧ��Ӧ����v��B��Ϊ_________mol/��L��min����
��3����ѧ����ʽ��XֵΪ__________ ��
��4���˷�Ӧ�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ����v��A��=5mol/��L��min������v��B��=6mol/��L��min������v��C��=4.5mol/��L��min������v��D��=8mol/��L��min����
���з�Ӧ����������__________�����ţ���
��1����Է�������Ϊ72������������һ�ȴ���ֻ��һ�֣��������Ľṹ��ʽΪ_________��
��2��ij��̬������һ��̬ϩ����ɵĻ��������ͬ�¡�ͬѹ�¶�����������ܶ�Ϊ13��ȡ��״���´˻������4.48 L��ͨ����������ˮ����ˮ��������2.8 g���������������Ϊ______________�������ʽ����
��3�� �л���Ľṹ���á�����ʽ����ʾ���磺![]() �ɼ�дΪ
�ɼ�дΪ![]()
![]() �ɼ�дΪ
�ɼ�дΪ ![]() ��õ�����ζ�����а����rϩ���rϩ�ļ���ʽ����ͼ��
��õ�����ζ�����а����rϩ���rϩ�ļ���ʽ����ͼ�� ���rϩ�ķ���ʽΪ___________��
���rϩ�ķ���ʽΪ___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com