
| A. | ①②⑤⑥ | B. | ①②④⑤ | C. | ②③⑤⑥ | D. | ③④⑤⑥ |
分析 ①质子数相同的一类原子总称为元素,元素的研究对象是原子;
②互为同位素原子,核外电子排布相同,最外层电子数决定化学性质;
③两种粒子,质子数一样,离子带电,离子的电子数一定和质子数不一样,分子不带电,分子的质子数和电子数一定相等,据此判断;
④质子数相同的原子为同种元素,元素的研究对象是原子;
⑤一种元素可以形成不同的单质;
⑥原子有质量数,元素没有质量数.
解答 解:①元素的研究对象是原子,质子数相同的粒子不一定属于同种元素,如CH4与H2O,若为原子则属于同种元素,故①错误;
②互为同位素原子,核外电子排布相同,最外层电子数决定化学性质,同位素的化学性质几乎完全相同,故②错误;
③分子显电中性,离子带电,两种粒子质子数和电子数均相同,如果一种为分子则质子数与电子数相等,一种为离子则质子数和电子数不相等,这样就与题设矛盾,所以不可能为一种分子、一种离子,故③正确;
④电子数相同的粒子不一定属于同种元素,如CH4与H2O,Na+与Mg2+,故④正确;
⑤一种元素可以形成不同的单质,如碳元素的单质有金刚石、石墨等,故⑤错误;
⑥元素没有质量数的概念,故⑥错误.
所以①②⑤⑥不正确.
故选A.
点评 本题考查同位素、质量数等基本概念,难度不大,注意把握同位素概念的内涵与外延.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 化学式 | 电离常数 |
| HF | Ka=3.5×10-4 |
| H2CO3 | Ka1=4.3×10-7 |
| Ka2=5.6×10-11 | |
| HClO | Ka=3.2×10-8 |
| A. | 同温同浓度下,溶液的pH值:NaF>NaClO>Na2CO3 | |
| B. | 结合H+的能力:ClO->CO32->F- | |
| C. | 碳酸钠溶液中加入少量氢氟酸的离子方程式:CO32-+2HF═2F-+H2O+CO2↑ | |
| D. | 次氯酸钠溶液中通入少量二氧化碳的离子方程式:ClO-+CO2+H2O═HCO3-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ZnC2水解生成乙烷(C2H6 ) | B. | Al4C3水解生成丙炔(C3H4) | ||
| C. | Mg2C3水解生成丙炔(C3H4) | D. | Li2C2水解生成乙烯(C2H4) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
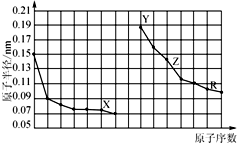
| A. | 同周期元素中,X的气态氢化物最稳定 | |
| B. | Y、Z的单质在空气中加热,均发生燃烧反应 | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子含有未成对电子最多的第二周期元素 | |
| B. | 位于元素周期表中第三周期ⅢA族的元素 | |
| C. | 原子最外层电子排布为2s22p6的元素 | |
| D. | 原子最外层电子排布为2s22p5的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入酸性高锰酸钾溶液中红色褪去 | |
| B. | 通入品红溶液中红色褪去 | |
| C. | 通入溴水中橙黄色褪去 | |
| D. | 通入氢氧化钠的酚酞溶液中红色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有② | B. | 只有②④ | C. | ②④⑤ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com