
【题目】溶液 A中可能含有如下离子:Na+、NH4+、Ba2+、Mg2+、SO42-、SO32-、Cl-、OH-。某同学设计并完成了如下的实验:

下列说法正确的是
A. 溶液 A 中一定存在 NH4+、 SO42-、 SO32-,可能存在 Na+
B. 溶液 A 中一定存在 NH4+、 Mg2+、 SO42-、 SO32-,可能存在 Cl-
C. 溶液 A 中可能存在 Cl-,且 c(Na+) ≥ 0.20 mol·L-1
D. 如果气体 F 能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有 NH4+
【答案】C
【解析】
溶液A中滴加过量BaCl2溶液所得沉淀B溶解于稀盐酸,部分溶解,并得到沉淀D为BaSO4,物质的是来0.01mol,溶解的质量为BaSO3,质量为2.17g,物质的量为0.01mol,由此推断原溶液中含有SO42-和SO32-,物质的量均为0.01mol;排除原溶液中含有Ba2+;滤液C中加入足量NaOH溶液,无沉淀可知溶液中无Mg2+,有气体放出,可知溶液中有NH4+,根据生成氨气448mL,可知溶液中NH4+的物质的量为0.02mol;溶液是电中性的,根据电荷守恒可知,溶液中一定还含有Na+,其物质的量为0.02mol,可能还含有Cl-;A.由分析可知,溶液 A 中一定存在 Na+,故A错误;B.由分析可知,溶液 A 中一定不存在 Mg2+,故B错误;C.由分析可知,溶液 A 中不存在 Cl-时Na+物质的量为0.02mol,若溶液 A 中存在 Cl-,Na+物质的量大于0.02mol,即 c(Na+) ≥ 0.20 mol·L-1,故C正确;D.氨气能使湿润的红色石蕊试纸变蓝,故D错误;答案为C。


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:

下列说法中正确的是( )
A.1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ
B.1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量
C.通常情况下,N2(g)和O2(g)混合能直接生成NO
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200 mL 1 mol/L的氯化铝溶液中加入一定体积的2 mol/L的NaOH溶液,最终产生7.8 g沉淀,则加入的NaOH溶液的体积可能是( )
① 350 mL ② 90 mL ③ 150 mL ④200 mL
A. 只有① B. ①③ C. ②④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上“中温焙烧——钠化氧化法”回收电镀污泥中的铬已获技术上的突破。其工艺流程如下:
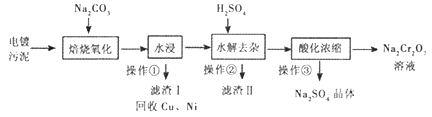
【查阅资料】
①电镀污泥中含有Cr(OH)3、Al203、ZnO、CuO、NiO等物质;水浸后溶液中含有Na2CrO4、NaAlO2、Na2ZnO2等物质;
②Na2CrO4转化成Na2Cr2O7离子反应方程式为:2 CrO42-+2H+=Cr2O72-+H2O;③Na2SO4、Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表:

请回答:
(1)操作①的名称是_______,“水浸”后的溶液呈_______性;
(2)“焙烧氧化”过程中Cr(OH)3转化成Na2CrO4的化学方程式为___________;
(3)滤渣II的主要成分有Zn(OH)2和X,生成X的离子反应方程式__________;
(4)“酸化浓缩”时,需继续加入H2SO4,然后_______、结晶、过滤。继续加入H2SO4目的是__________;
(5)以铬酸钠为原料,电化学法制备重铬酸钠的实验装置如图所示。
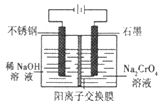
①阴极发生的电极反应式为:_____________;
②若测定阳极液中Na与Cr的物质的量之比值为d,则此时铬酸钠的转化率为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++OH-=H2O来表示的化学反应是( )。
A.CH3COOH+NaOH==CH3COONa+H2O
B.HNO3+KOH=KNO3+H2O
C.H2SO4+Ba(OH)2=BaSO4↓+2H2O
D.2HCl+Cu(OH)2=CuCl2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列各题:
(1)粘土[主要成分Al2Si2O5(OH)4] 是制备陶瓷的原料,请以氧化物形式表示粘土的组成_____________。
(2)现用四氯化硅和氮气在氢气中加强热发生反应,可制得高纯度氮化硅,反应的化学方程式为_________________________。
(3)雕花玻璃是用氢氟酸对玻璃进行刻蚀,这一过程中发生反应的化学方程式为_______。
(4)明矾可用于净水,请说明原因________________________。
(5)下图,若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在, B是白色胶状沉淀。

①实验室中常用A与某种溶液反应制备B,请写出该反应的离子方程式 _________________。
②A与C也可以反应生成B,请写出反应的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应 A2(g) +B2(g)=2AB(g) ΔH,其能量变化如图所示,下列叙述正确的是
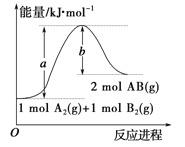
A. 断裂 1 mol A2 和 1 mol B2 中的化学键,放出a kJ 能量
B. ΔH=+(a-b)kJ·mol-1
C. 每生成 2 个AB分子吸收 b kJ 热量
D. 该反应中反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】任何一个化学反应中都会伴随能量变化和物质变化。
(1)下图为氢气和氧气生成1mol水蒸气时的能量变化情况。
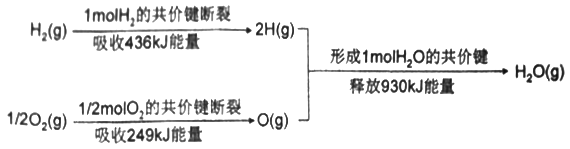
生成1mol水蒸气时,形成新化学键所释放的总能量_____断开旧化学键所吸收的总能量(填“大于”“小于”或“等于”),因此水的分解反应为________(填“吸热”或“放热”)反应。
(2)随着科学技术的发展和社会进步,各种各样的电器不断进入现代社会,化学电源大大丰富和方便了我们的生活、学习和工作。原电池中发生的化学反应属于______。镁铝原电池,电解质用稀硫酸,则其负极的电极反应式为______;电解质用氢氧化钠溶液,电池工作时,溶液中的OH-移向_____极(“镁”或“铝”)。
(3)在三个容器均为2L的密闭容器中发生反应:2HI(g) ![]() H2(g)+I2(g),已知H2(g)和I2(g)的起始物质的量均为0,HI(g)的物质的量(mol)随反应时间(min)的变化情况如下表所示,表中温度的单位为摄氏度(℃)。
H2(g)+I2(g),已知H2(g)和I2(g)的起始物质的量均为0,HI(g)的物质的量(mol)随反应时间(min)的变化情况如下表所示,表中温度的单位为摄氏度(℃)。
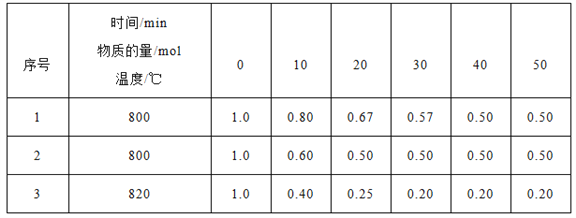
①实验1和实验2中,有一个实验使用了催化剂,则使用了催化剂的是实验_____(填“1”或“2”)。
②实验1中,20min~30min间生成I2(g)的平均反应速率为_____,实验3的反应达到化学反应限度时H2(g)物质的量的百分数为_______。
③下列物理量不再变化时,能判断实验3中反应达到化学反应限度的是__________。
A.混合气体颜色 B.混合气体密度 C.混合气体总压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在常温常压下:
①CH3CH2OH(l)+3O2(g)![]() 2CO2(g)+3H2O(g) ΔH1=-1366kJ·mol-1
2CO2(g)+3H2O(g) ΔH1=-1366kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2
③H2O(g)=H2O(l) ΔH3=-44kJ·mol-1
④CH3CH2OH(l)+2O2(g)![]() 2CO(g)+3H2O(l) ΔH4=-932kJ·mol-1
2CO(g)+3H2O(l) ΔH4=-932kJ·mol-1
则 CO的燃烧热 ΔH =_________。
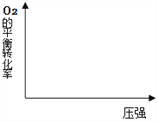
在图中画出,不同温度下(T1>T2),上述反应④中O2的平衡转化率随压强变化的关系图(请在图上标注温度T1、T2)。_________
(3)一定条件下,在体积为3 L的密闭容器中反应CO(g) + 2H2(g)![]() CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
①反应的平衡常数表达式K=__________;根据下图,升高温度,K值将___________(填“增大”、“减小”或“不变”)。

②500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是________。
③X点与Y点的平均速率:v(X)_________v(Y);其中X点的正反应速率v正(X)与Z点的逆反应速率v逆(Z)的大小关系为v正(X)________v逆(Z)(填“>”、“<”、“=”)。
④300℃时能够说明该可逆反应达到化学平衡状态的标志是____________ (填字母)。
a.v生成(CH3OH) = v生成(H2) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度相等
⑤500℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是___________。(填字母)
a.c(H2)减少 b.正反应速率加快,逆反应速率减慢
c.CH3OH 的百分含量增加 d.重新平衡时c(H2)/ c(CH3OH)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com