
| A. | 氧化还原反应一定有电子得失 | |
| B. | 置换反应一定是氧化还原反应 | |
| C. | 复分解反应一定不是氧化还原反应 | |
| D. | 有单质参与的化合反应和有单质生成的分解反应一定是氧化还原反应 |
分析 有电子得失或电子对的偏移的化学反应是氧化还原反应,由两种或两种以上的物质生成一种物质的反应是化合反应,由一种物质分解生成两种或两种以上物质的反应是分解反应,两种化合物相互交换成分生成另外两种化合物的反应是复分解反应,一种单质和一种化合物反应生成另外单质和化合物的反应是置换反应,据此分析解答.
解答 解:A.氧化还原反应的实质是有电子的得失或电子对的偏移,所以氧化还原反应中一定有电子得失或电子对的偏移,故A错误;
B.单质变为化合物或化合物变为单质,一定有电子的转移,所以置换反应一定是氧化还原反应,故B正确;
C.复分解反应中各元素的化合价都不发生变化,所以一定不是氧化还原反应,故C正确;
D.有单质参加的化合反应和有单质生成的分解反应,一定有元素化合价的变化,所以一定是氧化还原反应,故D正确;
故选A.
点评 本题考查了氧化还原反应、分解反应等概念,明确这几个概念之间的关系是解本题的关键,注意这几个概念的区别.


科目:高中化学 来源: 题型:填空题
 甲醇(CH3OH)燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
甲醇(CH3OH)燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
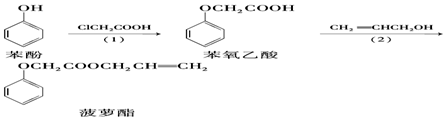
| A. | 步骤(1)产物中残留的苯酚可用FeCl3溶液检验 | |
| B. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| C. | 苯氧乙酸分子中含有醚键、羧基两种官能团 | |
| D. | 步骤(2)产物中残留的烯丙醇可用溴水检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
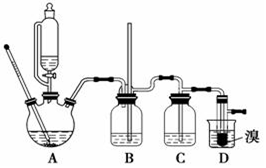 实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH→CH2=CH2$\stackrel{Br_{2}}{→}$BrCH2CH2Br用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH→CH2=CH2$\stackrel{Br_{2}}{→}$BrCH2CH2Br用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 碱 | 酸 | 盐 | 酸性氧化物 | |
| A | 纯碱 | 硝酸 | 烧碱 | 二氧化硫 |
| B | 苛性钠 | 硫酸 | 胆矾 | 氧化铜 |
| C | 烧碱 | 醋酸 | 纯碱 | 三氧化硫 |
| D | 氢氧化钡 | 碳酸 | 小苏打 | 水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤④①③ | B. | ④①②⑤③ | C. | ①④②⑤③ | D. | ⑤②①④③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol/L | B. | 1 mol/L | C. | 0.01 mol/L | D. | 0.22 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com