
| A、工业上用铁矿石炼铁 |
| B、用稀盐酸除去钢铁表面的铁锈 |
| C、工业上煅烧石灰石制生石灰 |
| D、用胃舒平(氢氧化铝)治疗胃酸过多 |


科目:高中化学 来源: 题型:

| n(Fe3+) |
| n(Fe2+) |
| n(Fe3+) |
| n(Fe2+) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| LiBH4 |
| THF |
| LiBH4 |
| THF |
| CH3I |
| 催化剂 |
| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| +W |
| +W |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
A~G是几种烃的分子球棍模型(如图),据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、30 | B、42 | C、45 | D、60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液:Al3+、K+、Cl-、S2- |
| B、滴加酚酞显红色的溶液:Na+、ClO-、NO3-、Cl- |
| C、滴加甲基橙显红色的溶液:Fe2+、NH4+、SO42-、NO3- |
| D、c(H+)=c(OH-)的溶液:Fe3+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
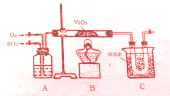 某研究性学习小组为在实验室再现二氧化硫催化氧化的过程,应制取少量二氧化硫晶体,设计了如下图所示装置,已知三氧化硫通水生成硫酸并放出大量热,容易形成酸液,试回答:
某研究性学习小组为在实验室再现二氧化硫催化氧化的过程,应制取少量二氧化硫晶体,设计了如下图所示装置,已知三氧化硫通水生成硫酸并放出大量热,容易形成酸液,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
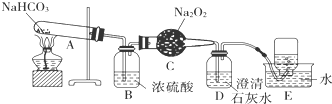
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com