
| A. | 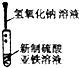 制备氢氧化亚铁 | B. | 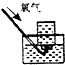 收集氧气 | ||
| C. |  制备并检验氢气的可燃性 | D. | 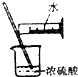 浓硫酸稀释 |
科目:高中化学 来源: 题型:选择题
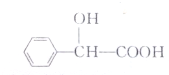 某有机物的结构如下所示,有关该物质的说法错误的是( )
某有机物的结构如下所示,有关该物质的说法错误的是( )| A. | 该物质的分子式为C8H8O3 | |
| B. | 该物质分子中的8个碳原子都在同一个平面上 | |
| C. | 该物质既可以发生酯化反应又可以发生缩聚反应 | |
| D. | 1mol该物质可以与2mol金属Na反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
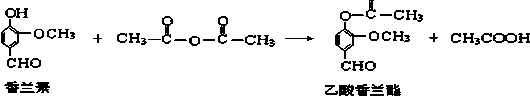
| A. | 该反应属于加成反应 | |
| B. | FeCl3溶液可用于区别香兰素与乙酸香兰酯 | |
| C. | 乙酸香兰酯的分子式为C10H8O4 | |
| D. | 乙酸香兰酯在足量NaOH溶液中水解得到乙酸和香兰素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4mol/L | B. | 1.4mol/L | C. | 1.2mol/L | D. | 0.7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
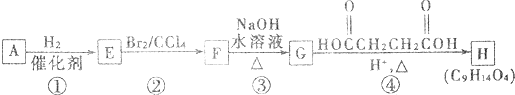
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 时间/min | 0 | 20 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.020 | 0.020 | 0.020 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤⑦ | B. | ②③④⑤⑥ | C. | ③④⑥ | D. | ②③④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com