
| A. | 镁、铝在常温下都能被氧气氧化 | |
| B. | 将氯化铝和硫酸铝溶液蒸干灼烧后均得到氧化铝 | |
| C. | Na2O2与水反应,红热的铁与水蒸气反应均能生成碱 | |
| D. | Fe(OH)3不溶于水不能通过化合反应直接得到 |
分析 A.镁和铝在常温下都能被氧气氧化,形成致密的氧化薄膜;
B.氯化铝溶液中铝离子水解生成氢氧化铝和盐酸,溶液显酸性,水解过程为吸热反应,加热促进水解,蒸干得到水解产物,灼烧时生成的氢氧化铝分解生成氧化铝,硫酸铝溶液中铝离子水解,反应生成硫酸和氢氧化铝,水解过程为吸热反应,加热促进水解,蒸干是蒸发的水,最后得到硫酸铝固体;
C.铁和水蒸气高温反应生成四氧化三铁和氢气;
D.氢氧化铁可以通过化合反应生成,氢氧化亚铁和空气中氧气、水蒸气发生反应生成氢氧化铁;
解答 解:A.镁和铝在常温下都能被氧气氧化形成致密的氧化薄膜,常温下都能被氧气氧化,故A正确;
B.氯化铝溶液中铝离子水解生成氢氧化铝和盐酸,溶液显酸性,AlCl3+3H2O?Al(OH)3+3HCl,水解过程为吸热反应,加热促进水解,蒸干HCl挥发促进水解正向进行得到水解产物Al(OH)3,灼烧时生成的氢氧化铝分解生成氧化铝,2Al(OH)3 $\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3O2↑,硫酸铝溶液中铝离子水解,反应生成硫酸和氢氧化铝,反应的化学方程式为:Al2(SO4)3+6H2O?2Al(OH)3+3H2SO4,水解过程为吸热反应,加热促进水解,蒸干蒸发的是水,最后得到固体硫酸铝,故B错误;
C.Na2O2与水反应生成氢氧化钠和氧气,生成产物氢氧化钠为碱,红热的铁与水蒸气反应生成四氧化三铁和氢气,3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,不能生成碱,故C错误;
D.Fe(OH)3不溶于水,但能通过化合反应直接得到,如4Fe(OH)2+O2+2H2O=4Fe(OH)3,故D错误;
故选A.
点评 本题考查了物质的性质、盐类水解原理,主要是过氧化钠、铁、氢氧化铁等物质的性质应用,掌握基础是解题关键,题目难度中等.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即盖上盖板,用环形玻璃搅拌棒不断搅拌,准确读出反应体系的最高温度 | |
| B. | 实验事实证明乙酸乙酯中少量乙醇可以用水洗方法除去,其原理与溴水中加四氯化碳萃取溴类似 | |
| C. | 油脂制肥皂实验中加乙醇的目的是增大油脂的溶解度,加快油脂皂化反应速率 | |
| D. | 当高锰酸钾晶体结块时,应在研钵中用力研磨,以得到细小晶体,有利于加快反应或溶解的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯的结构式:C7H8 | B. | 乙烷的结构简式:CH3CH3 | ||
| C. | 甲醇的电子式:CH3OH | D. | 乙醇的分子式:CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
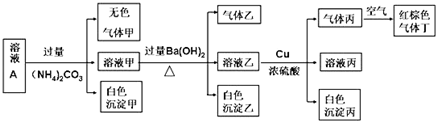
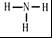 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 | B. | CO2 | C. | Cl2 | D. | O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
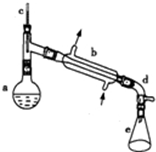 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示.可能用到的有关数据如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示.可能用到的有关数据如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环乙醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
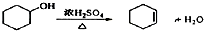 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH3在该反应中作还原剂,被氧化 | |
| B. | Si3N4具有硬度大、熔点高,说明Si3N4可用作耐高温材料 | |
| C. | 标准状况下,22.4LNH3所含原子总数目为4×6.02×1023 | |
| D. | 该反应每生成1mol Si3N4转移电子总数目为12×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2ml0.3mol/L的硅酸钠溶液中滴入稀盐酸所制得的硅酸胶体中胶粒的数目为0.0006NA | |
| B. | 常温下,1LpH=2的H2S溶液中H+的数目为0.01NA | |
| C. | 1mol铁粉与22.4L(标准状况)氯气充分反应,转移的电子数是3NA | |
| D. | 常温常压下,2.8gC4H8中有1.2NA的共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com