
(16分) 硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
查阅资料 ①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃;②2B+6HCl△2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
设计实验 某同学设计如图所示装置制备三氯化硼:

请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同。写出高锰酸钾固体粉末与浓盐酸反应的离子方程式: _____。
(2)E装置的作用是 。如果拆去B装置,可能的后果是 。
(3)实验中可以用一个盛装 (填试剂名称)的干燥管代替F和G装置,使实验更简便。
(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式: ;实验室保存三氯化硼的注意事项是 。
(5)为了顺利完成实验,正确的操作是 (填序号).
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓 (填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
(1) 2MnO4-+10Cl-+16H+ = 2Mn2++8H2O+5Cl2↑
(2)冷却和收集三氯化硼 ;硼粉与氯化氢反应生成的产物中有氢气,加热氢气与氯气的混合气体,易发生爆炸;(3)碱石灰 ;(4)BCl3+3H2O=H3BO3+3HCl↑ 密封保存
(5) ① ;(6)NaOH
【解析】
试题分析:(1)在A装置中用高锰酸钾固体粉末与浓盐酸发生反应可以制取氯气,反应的方程式为:2MnO4-+10Cl-+16H+ = 2Mn2++8H2O+5Cl2↑。(2)由于浓盐酸有挥发性,所以在氯气中含有HCl气体,用饱和NaCl溶液除去HCl杂质,用浓硫酸进行干燥,在D中发生反应:3Cl2+2B 2BCl3;在 E装置的作用是冷却和收集三氯化硼 ;如果拆去B装置,可能会发生反应2B+6HCl△2BCl3↑+3H2↑,在D中加热氢气与氯气的混合气体,易发生爆炸;后果是多余的氯气用NaOH溶液吸收。为防止倒吸及BCl3水解在E与G之间连接一个盛有浓硫酸的装置。在实验中也可以用一个盛装碱石灰的干燥管代替F和G装置,使实验更简便。(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,该反应的化学方程式是BCl3+3H2O=H3BO3+3HCl↑;因此在实验室保存三氯化硼的注意事项要密封保存,防止受潮水解。(5)①先点燃A处酒精灯,待整套装置中都充满Cl2后再点燃D处酒精灯,使之发生反应。正确。②若先点燃D处酒精灯,这时B就与装置中的空气发生反应得到B2O3,再点燃A处酒精灯也不能产生BCl3了。错误。③同时点燃A、D处酒精灯也会导致产生B2O3,影响制备BCl3。(6)由于B的性质与Al相似,既能与强酸反应,也能与强碱反应放出氢气,所以取少量样品于试管中,滴加浓NaOH溶液,若有气泡产生,则样品中含有硼粉。
2BCl3;在 E装置的作用是冷却和收集三氯化硼 ;如果拆去B装置,可能会发生反应2B+6HCl△2BCl3↑+3H2↑,在D中加热氢气与氯气的混合气体,易发生爆炸;后果是多余的氯气用NaOH溶液吸收。为防止倒吸及BCl3水解在E与G之间连接一个盛有浓硫酸的装置。在实验中也可以用一个盛装碱石灰的干燥管代替F和G装置,使实验更简便。(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,该反应的化学方程式是BCl3+3H2O=H3BO3+3HCl↑;因此在实验室保存三氯化硼的注意事项要密封保存,防止受潮水解。(5)①先点燃A处酒精灯,待整套装置中都充满Cl2后再点燃D处酒精灯,使之发生反应。正确。②若先点燃D处酒精灯,这时B就与装置中的空气发生反应得到B2O3,再点燃A处酒精灯也不能产生BCl3了。错误。③同时点燃A、D处酒精灯也会导致产生B2O3,影响制备BCl3。(6)由于B的性质与Al相似,既能与强酸反应,也能与强碱反应放出氢气,所以取少量样品于试管中,滴加浓NaOH溶液,若有气泡产生,则样品中含有硼粉。
考点:考查气体的制取、净化、干燥、加热的先后顺序、盐的水解、物质的保存、物质的检验方法。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:2013-2014重庆市下学期期中考试高二化学试卷(解析版) 题型:选择题
下列有关原电池的说法中,正确的是( )
A.铝片和镁片用导线连接后插入NaOH溶液中,镁片较活泼,作负极
B.铝片和铜片用导线连接后插入浓硝酸中,铜作负极
C.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀
D.将反应2Fe3++Fe=3Fe2+设计为原电池,则可用锌片作负极,铁片作正极,FeCl3溶液作电解质
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市5月高三月考理综化学试卷(解析版) 题型:选择题
下列实验操作与预期的实验目的或结论均正确的是
选项 | 实验操作 | 预期的实验目的或结论 |
A | 对某白色固体进行焰色反应实验,火焰呈黄色 | 该物质为钠盐 |
B | SO2通入某红色溶液中,溶液褪色 | 该溶液为品红溶液 |
C | 蔗糖溶液中加入少量稀硫酸加热,然后加银氨溶液再加热 | 验证蔗糖在强酸性条件下是否发生水解 |
D | pH均为1的盐酸、醋酸溶液分别用蒸馏水稀释m倍、n倍后的pH相同 | m<n |
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市高三5月月考理综化学试卷(解析版) 题型:实验题
(12分)为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)实验过程如下:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4.
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中的溶液变黄时,停止加热,夹紧弹簧夹K2.
Ⅳ.打开活塞b,使约2ml的溶液流入D试管中,检验其中的离子.
V.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.
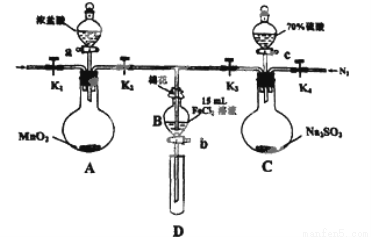
(1)过程Ⅰ的目的是______________________。
(2)棉花中浸润的溶液为__________________。
(3)A中发生反应的化学方程式为__________________________________。
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是______________
(5)过程Ⅵ中检验B溶液中是否含有硫酸根的操作是________________________________
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程IV B溶液中含有的离子 | 过程VI B溶液中含有的离子 |
甲 | 有Fe3+无Fe2+ | 有SO42﹣ |
乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市高三5月月考理综化学试卷(解析版) 题型:选择题
萨罗(Salo1)是一种消毒剂,属于芳香族含氧衍生物,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等)。则下列说法不正确的是:
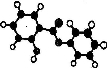
A.萨罗的分子式为Cl3Hl0O3
B.1mol萨罗与浓溴水反应,需要消耗3mol Br2
C.1mol萨罗发生水解,需要消耗3mol NaOH
D.萨罗经水解、分离、提纯可得到纯净的苯酚和水杨酸(邻羟基苯甲酸)
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市六校高三5月第三次诊断性考试理综化学试卷(解析版) 题型:选择题
4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8,下列说法不正确的是
A.与W相邻的同主族元素可制成重要的半导体材料
B.元素原子半径从大到小的顺序是X、Y、Z
C.WZ4分子中W、Z原子通过共价键结合且最外层均达到8电子结构
D.W、Y、Z元素对应的氢化物稳定性最强的是H2Y
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市主城七区高三下学期第二次联考理综化学试卷(解析版) 题型:简答题
(14分)A、B、C、D、E、F是原子序数依次增大的六种短周期元素。F的单质在D2中燃烧的产物可使品红溶液褪色;B的单质在D2中燃烧可生成BD和BD2两种气体;E的原子序数为B的两倍;A元素的一种核素中不含中子。请回答下列问题:
(1)C的单质分子的结构式为 ;ED的电子式为 。
(2)E单质在BD2中剧烈燃烧生成黑白两种固体,该反应的化学方程式为 。
(3)FD2气体通入BaCl2和HNO3的混合溶液中,生成白色沉淀和无色气体CD,有关反应的离子方程式为 ,由此可知CD和FD2中还原性较强的是 (填化学式)。
(4)A、C、D、F四种元素按原子个数比为5 :1 :4 :1形成化合物甲,则甲的化学式为 。将0.01mol/L的甲溶液与0.03mol/L的Ba(OH)2溶液等体积混合得到沉淀,已知该沉淀的Ksp=x ,则混合溶液中酸根离子的浓度为 mol / L(用含x的代数式表示,混合后溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期高三第二次诊断测试理科综合化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A.在反应中消耗1mol Cl2,转移的电子数一定为2NA。
B.标准状况下,0.5mol氦气含有的电子数为NA
C.15g CH3+(碳正离子)中含有电子数为10NA
D.0.1L 2mol·L﹣1的(NH4)2S溶液中含有的S2﹣数目为0.2NA
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
(原创)能用键能大小解释的是
A.稀有气体一般很难发生化学反应
B.常温常压下,氟气的密度小于氯气
C.相同条件下,NH3在水中的溶解度大于PH3
D. SiC晶体的熔点比晶体硅的高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com