
| A. | 氧化铝陶瓷、氮化硅陶瓷都属于新型无机非金属材料 | |
| B. | 煤矿井下的瓦斯爆炸主要是氢气燃烧引起的 | |
| C. | 乙烯的产量是衡量一个国家石油化工发展水平的标志 | |
| D. | 在粉尘较多的工作场所,工作人员易患硅肺病 |
分析 A.新型无机非金属材料主要有先进陶瓷、非晶体材料、人工晶体、无机涂层、无机纤维等;
B.煤矿矿坑中的可燃性气体是甲烷;
C.乙烯主要用于制造塑料、合成纤维、有机溶剂等,是石油化工发展的标志;
D.粉尘含有二氧化硅.
解答 解:A.氧化铝陶瓷、氮化硅陶瓷属于新型无机非金属材料,故A正确;
B.煤矿矿坑中的可燃性气体是甲烷,不是氢气,故B错误;
C.乙烯工业的发展,带动了其它以石油为原料的石油化工的发展.因此一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志,故C正确;
D.粉尘含有二氧化硅,在粉尘较多的工作场所,工作人员易患硅肺病,故D正确.
故选B.
点评 本题考查无机非金属材料、有机物的性质和环境污染,难度不大,学生应熟悉材料中的成分,能运用所学化学知识来解决实际问题.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:解答题
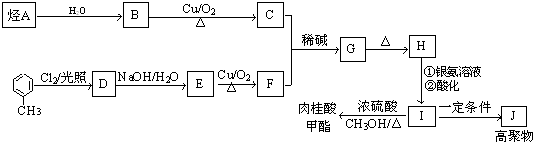
 +CH3CHO$\stackrel{稀碱}{→}$
+CH3CHO$\stackrel{稀碱}{→}$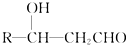 $→_{△}^{-H_{2}O}$RCH=CHCHO
$→_{△}^{-H_{2}O}$RCH=CHCHO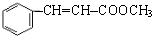 ;J的结构简式为
;J的结构简式为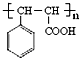 ;
; 、
、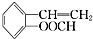 、
、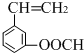 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
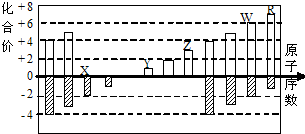 如图是部分短周期元素化合价与原子序数的关系图
如图是部分短周期元素化合价与原子序数的关系图| A. | 离子半径比较:W>R>X>Y>Z | |
| B. | W的气态氢化物的还原性和稳定性均弱于R的氢化物 | |
| C. | 工业上电解熔融的ZR3制备Z单质 | |
| D. | 含Y元素的盐溶液可能显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 试剂或材料 | 操作 | |
| A | 淀粉溶液 | NaCl | 半透膜 | 渗析 |
| B | 苯 | 苯酚 | 浓溴水 | 过滤 |
| C | 乙醇 | 水 | 生石灰 | 蒸馏 |
| D | 乙酸乙脂 | 乙醇 | 饱和Na2C03溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中一定存在分子间作用力,不一定有共价键 | |
| B. | 元素的非金属性越强,其单质的活泼性越强 | |
| C. | 含有金属阳离子的晶体不一定是离子晶体,离子晶体中一定含金属阳离子 | |
| D. | 溶于水后可电离出能自由移动离子的晶体一定是离子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| A. | X、Z、W的简单氢化物的稳定性Z>W>X | |
| B. | W元素的单质在化学反应中只表现还原性 | |
| C. | Y、Z、W的最高价氧化物均能与NaOH溶液反应 | |
| D. | X、Y的简单离子半径Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验目的 | 实验编号 | 温度 | 金属铝形态 | 酸及其浓度 |
| 1.实验Ⅰ和Ⅱ探究盐酸浓度对该反应速率的影响 2.实验Ⅱ和Ⅲ探究:③ 3.实验Ⅱ和Ⅳ探究金属规格(铝片、铝粉)对该反应速率的影响 4.Ⅰ、Ⅱ、Ⅲ实验探究铝与稀盐酸和稀硫酸反应的差异 | Ⅰ | 25℃ | 铝片 | 4.0moL/L盐酸 |
| Ⅱ | 25℃ | 铝片 | 2.0mol•L-1盐酸 | |
| Ⅲ | 35℃ | 铝片 | 2.0mol•L-1盐酸 | |
| Ⅳ | 25℃ | 铝片 | 2.0moL/L盐酸 | |
| Ⅴ | 25℃ | 铝片 | 2.0mol•L-1硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氮元素是地球上含量很丰富的一种元素,其单质和化合物对我们的环境和生命有重要的意义.
氮元素是地球上含量很丰富的一种元素,其单质和化合物对我们的环境和生命有重要的意义.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将纯铁片放入稀硫酸中,反应缓慢,再加入少量硫酸溶液,可加快产生氢气的速率 | |
| B. | 用锌片和稀硫酸反应制取氢气时,改用98%的浓硫酸可加快产生氢气的速率 | |
| C. | 反应2H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 | |
| D. | 稀盐酸跟锌片反应,加入少量的氯化钠固体,反应速率不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com