
| A. | 25.4ρ | B. | 12.7ρ | C. | 6.97ρ | D. | 6.35ρ |
分析 发生反应:HCl+AgNO3═AgCl↓+HNO3,生成沉淀的质量与原盐酸的质量相等,假设AgCl为143.5g,则盐酸为143.5g,根据V=$\frac{m}{ρ}$计算盐酸的体积,根据方程式计算盐酸中HCl的质量,再根据n=$\frac{m}{M}$计算HCl的物质的量,根据c=$\frac{n}{V}$计算盐酸物质的量浓度.
解答 解:发生反应:HCl+AgNO3═AgCl↓+HNO3,生成沉淀的质量与原盐酸的质量相等,假设AgCl为143.5g,则盐酸为143.5
由HCl+AgNO3═AgCl↓+HNO3,可知HCl的质量为36.5g,则其物质的量为$\frac{36.5g}{36.5g/mol}$=1mol,
盐酸的体积为$\frac{143.5g}{1000ρg/L}$=$\frac{143.5}{1000ρ}$L,
故盐酸物质的量浓度为$\frac{1mol}{\frac{143.5}{1000ρ}L}$=6.97ρ mol•L-1,故选C.
点评 本题考查化学方程式有关计算、物质的量浓度计算,属于无数据型计算,注意利用特殊值赋值法简化计算,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 铁制品锈蚀时主要发生析氢腐蚀 | |
| B. | 施用适量石膏可以降低盐碱地(含较多NaCl、Na2CO3)的碱性 | |
| C. | 电镀厂未经处理的废水可以直接用来灌溉农田 | |
| D. | 将水坝的钢铁闸门与直流电的正极相连可以防闸门腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.4 g乙烯与丙烯的混合气体含有NA个碳原子 | |
| B. | 精炼铜,若阳极失去2NA个电子,则阴极增重64 g | |
| C. | 在1 L 0.1mol/L 的Na2CO3溶液中,阴离子总数小于0.1NA | |
| D. | 将1 L 2 mol/L 的FeCl3溶液加入到沸水中,加热使之完全反应,所得氢氧化铁胶体粒子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO+H2O(g)═CO2+H2 | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | 2F2+2H2O═4HF+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
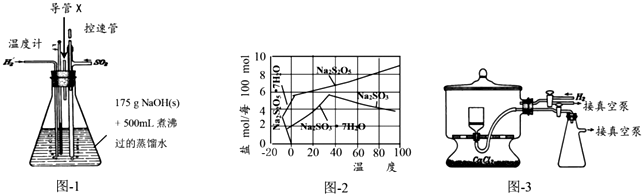
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有SO2、NH3和NO | B. | 一定有NO和HCl | ||
| C. | 可能有Cl2和O2 | D. | 一定没有Cl2、NO2、NH3和O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2 | B. | 2:3 | C. | 4:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com