
【题目】下列事实对应的离子方程式或电极反应式书写正确的是( )
A. 用石墨作电极电解CuSO4溶液2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
B. 碳酸钠溶液显碱性:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
C. 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
D. 在强碱溶液中Fe(OH)3与NaClO反应生成Na2FeO4:3ClO-+2 Fe(OH)3=2FeO42-+3Cl-+H2O+4H+
科目:高中化学 来源: 题型:
【题目】下图为合成氨反应(N2+ 3H2![]() 2NH3 ΔH<0 )中氮气反应速率v(N2)变化的图象,则横坐标不可能的是
2NH3 ΔH<0 )中氮气反应速率v(N2)变化的图象,则横坐标不可能的是

A. 温度(T/K) B. 压强(P/Pa)
C. 反应时间(t/min) D. 氮气浓度(c/mol·L―1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A与CO、H2O以物质的量1︰1︰1的比例形成B,B中的两个官能团分别具有乙烯和乙酸中官能团的性质,E是有芳香气味、不易溶于水的油状液体,有关物质的转化关系如下:
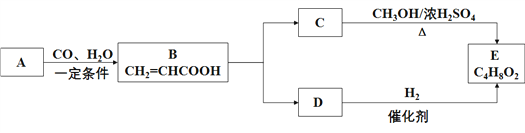
请回答:
(1)A的结构简式__________。
(2)D→E的反应类型__________。
(3)CE的化学方程式________________________________________。
(4)下列说法不正确的是__________。
A.可用金属钠鉴别B和C
B.A在一定条件下可与氯化氢发生加成反应
C.乙酸和乙醇在浓硫酸作用下加热也可生成E
D.与A的最简式相同,相对分子质量为78的烃一定不能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将3 molCO2和2 mol H2混合于2 L恒容密闭容器中,发生如下反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)。回答下列问题:
CO(g)+H2O(g)。回答下列问题:
(1)该反应的化学平衡常数表达式K=__________________________。
(2)已知700℃时,该反应的平衡常数K1=0.60,则该温度下反应CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
的平衡常数K2=____________,反应![]() CO2(g)+
CO2(g)+ ![]() H2(g)
H2(g)![]()
![]() CO(g)+
CO(g)+ ![]() H2O(g)的平衡常数K3=___________。
H2O(g)的平衡常数K3=___________。
(3)已知在1000℃时,该反应的平衡常数K4=1.0,则该反应为_________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是____________(填标号)。
a. 容器中压强不变 b.c(CO2)=c(CO)
c.CO2的生成速率等于H2的消耗速率 d.混合气体的平均相对分子质量不变
(5)在1000℃下,将3 molCO2和2 mol H2混合于2 L恒容密闭容器中,发生如下反应:CO2(g)+ H2(g)![]() CO(g)+ H2O(g),某时刻CO2的物质的量为2.0 mol,则此时v(正)__________v(逆) (填“>”“<”或“=”);该温度下反应达到平衡时,CO2的转化率为____________________。
CO(g)+ H2O(g),某时刻CO2的物质的量为2.0 mol,则此时v(正)__________v(逆) (填“>”“<”或“=”);该温度下反应达到平衡时,CO2的转化率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分石灰是______________(填化学式),石灰所属的物质类型__________________(填序号)。
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂 ⑤纯净物 ⑥化合物 ⑦盐
(2)生石灰可做干燥剂的理由是________________________(用化学方程式表示)。
(3)你认为下列内容还必须在这种小纸袋上注明的是____________(填序号)。
①禁止食用 ②可以食用 ③禁止未成年人用手拿 ④生产日期
(4)小纸袋中的物质能否长期地作干燥剂?为什么?_______________________________。
(5)某同学将浓硫酸、氢氧化钠固体、生石灰等物质划分为一类。该同学的分类依据为____________(填字母)。
A. 酸类 B. 碱类 C. 氧化物 D. 干燥剂
(6)生石灰还可以跟哪些类别的物质发生化学反应?请列举三例并填表。__________________、__________________、__________________、__________________、__________________、__________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究不溶性盐X(仅含四种元素)的组成和性质,设计并完成如下实验:

请回答:
(1)X的组成元素为H、O和______(用元素符号表示),化学式为________________。
(2)写出经一步反应能得到X的化学方程式(要求非氧化还原反应)
_______________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐中常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为________(只填化学式)。
②分离操作①中所用到的玻璃仪器有____________。
③洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为________。
(2)用提纯的NaCl配制450 mL 4.00 mol·L-1NaCl溶液,所用仪器除药匙、烧杯、玻璃棒外还有________(填仪器名称)。
(3)在实验中多次用到玻璃棒,其作用有三个,分别是______________、______________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )




![]()
A. 用a制备并收集氨气 B. 用b制备并检验乙炔
C. 用c蒸馏海水得到淡水 D. 用d分离Na2CO3溶液与植物油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】索氏提取法是测定动植物样品中粗脂肪含量的标准方法。其原理是利用如图装置,用无水乙醚等有机溶剂连续、反复、多次萃取动植物样品中的粗脂肪。具体歩驟如下:
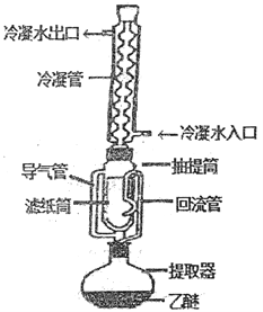
①包装:取滤纸制成滤纸管,放入烘箱中干燥后,移至仪器X中冷却至室温。然后放入称量瓶中称量,貭量记作a;在滤纸筒中包入一定质量研细的样品,放入烘箱中干燥后,移至仪器X中冷却至室温,然后放入称量瓶中称量,貭量记作b.
②萃取:将装有样品的滤纸筒用长镊子放入抽提筒中,注入一定量的无水乙醚,使滤纸筒完全浸没入乙醚中,接通冷凝水.加热并调节温度,使冷凝下滴的无水乙醚呈连珠状,至抽提筒中的无水乙醚用滤纸点滴检查无油迹为止(大约6h~12h).
③称量.萃取完毕后,用长镊子取出滤纸筒,在通风处使无水乙醚挥发后,将滤纸筒放入烘箱中干燥后,移至仪器X中冷却至室温.然后放入称量瓶中称量,貭量记作c。
回答下列问题:
(1)实验中使用了三次的仪器X的名称________。为提高乙醚蒸气的冷凝效果,索氏提取器中的冷凝管可选用下列(______)
A.空气冷凝管![]()
B.直形冷凝管![]()
C.蛇形冷凝管![]()
(2)①实验中必须十分注意乙醚的安全使用,如不能用明火加热、室内保持通风等。为防止乙醚挥发到空气中形成燃爆,常在冷凝管上口连接一个球形干燥管,其中装入的药品为____(填字母)。
A.活性炭 B.碱石灰 C.P2O5 D.浓硫酸
②无水乙醚在空气中可能氧化生成少量过氧化物,加热时发生爆炸。检验无水乙醚中是否含有过氧化物的方法是__________。
(3)①实验中需控制温度在70℃~80℃之间,考虑到安全等因素,应采取的加热方式是____。
②当无水乙醚加热沸腾后,蒸气通过导气管上升,被冷凝为液体滴入抽提管中,当液面超过回流管最高处时,萃取液即回流入提取器(烧瓶)中……该过程连续、反复、多次进行,则萃取液回流入提取器(烧瓶)的物理现象为_______。
A.冷凝回流 B.虹吸 C.倒吸 D.分液
③索氏提取法与一般萃取法相比较,其优点为______。
(4)数据处理:样品中纯脂肪百分含量____(填“>”、“<”或“=”)![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com