
| A. | 电解氯化钠溶液制金属钠 | B. | 石灰石是炼铁和制玻璃的原料之一 | ||
| C. | 氯气通入石灰乳中制漂白粉 | D. | 工业炼铁的主要设备高炉 |
分析 A、金属钠化学性质非常活泼,电解氯化钠溶液无法得到金属钠,必须是电解熔融氯化钠才能得到金属钠;
B、炼铁是将原料(铁矿石、焦炭、石灰石)通入高炉中,在高炉中发生复杂反应,生成铁的单质;普通玻璃的原料有:砂子,石灰石和纯碱;
C、漂白粉的主要成分为氯化钙、次氯酸钙,是氯气与氢氧化钙反应产物;
D、工业炼铁的主要设备高炉;
解答 解:A、电解氯化钠溶液生成氢氧化钠、氯气和氢气,无法得到金属钠,必须通过电解熔融氯化钠获得金属钠和氯气,故A错误;
B、炼铁材料为铁矿石、焦炭、石灰石,普通玻璃的原料有:砂子,石灰石和纯碱,所以石灰石是炼铁和制玻璃的原料之一,故B正确;
C、氯气与氢氧化钙反应生成次氯酸钙、氯化钙和水,其中氯化钙和次氯酸钙为漂白粉的主要成分,故C正确;
D、工业炼铁的主要设备高炉,故D正确;
故选A.
点评 本题考查了金属冶炼的一般原理、炼铁的设备、氯气的化学性质、炼铁的主要原料,题目难度中等,注意掌握常见金属的冶炼方法,较活泼的金属,如钠、镁、铝等,提纯采用电解方法冶炼.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 括号内为杂项 | 除杂试剂 | 除杂操作 | |
| A | Na2O2(Na2O) | O2 | 在纯氧中加热 |
| B | Na2CO3(NaHCO3) | CO2 | 通入过量的CO2 |
| C | FeCl(FeCl2) | Cl2 | 通入过量的Cl2 |
| D | FeSO4(CuSO4) | Fe | 加入过量的Fe粉,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴水褪色 | B. | 乙醇与浓硫酸共热至170℃ | ||
| C. | 溴乙烷与NaOH水溶液共热 | D. | 在液溴与苯的混合物中撒入铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
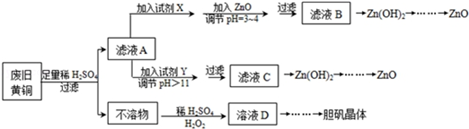
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| s沉淀完全的pH | 3.0 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电器起火,立即用水扑灭 | |
| B. | 炒菜时油锅着火,立即盖上锅盖 | |
| C. | 厨房煤气管道漏气,立即关闭阀门并开窗通风 | |
| D. | 图书管内图书着火,立即用液态二氧化碳灭火器扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0mol/L的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| B. | 甲基橙呈红色的溶液:NH4+、Ba2+、[Al(OH)4]-、Cl- | |
| C. | pH=12的溶液:K+、Na+、CH3COO-、Br- | |
| D. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 大理石和醋酸:CO32-+2H+═H2O+CO2↑ | |
| C. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| D. | 向Ba(OH)2溶液中滴加KHSO4溶液至中性:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| B. | 1.7g氨气所含分子数目为0.1NA | |
| C. | 1L 1mol•L-1的Na2SO4溶液中含有Na+的个数为NA | |
| D. | 2g氢气所含氢原子数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com