
【题目】为了探究金属单质M与盐溶液的反应,某同学进行了下列实验,实验过程及现象如图所示,结合实验现象判断该同学得出的下列结论中正确的是

A. 向滤液中滴加盐酸的实验现象是产生白色沉淀
B. 滤渣可能是两种单质的混合物
C. 滤渣在足量的稀硝酸中能完全溶解
D. 加入的金属M可能是镁或钠
【答案】C
【解析】
充分反应后得到无色溶液,说明硝酸铜和硝酸银已经完全反应;
向滤渣中加入稀盐酸,产生无色气体,说明滤渣中含有金属M,即金属M是过量的;
向滤液中滴加稀盐酸时,不可能产生白色沉淀,因为能和氯离子结合成白色沉淀的只有银离子,滤液中不含有银离子。
A、向滤液中滴加盐酸的实验现象不可能是产生白色沉淀,因为滤液中不含有银离子,加入稀盐酸时,不可能产生白色沉淀,故A错误;
B、滤渣中一定含有单质银、铜和M,故B错误;
C、滤渣中一定含有单质银、铜和M,M活泼些大于铜和银,所以滤渣在足量的稀硝酸中能完全溶解,故C正确;
D、加入的金属M不是单质钠,因为钠和硝酸银、硝酸铜溶液的反应是钠和水反应生成氢氧化钠和氢气,氢氧化钠和铜离子、银离子生成沉淀,加入盐酸无气体生成,故D错误;
故选:C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】标准状况下,三个干燥烧瓶分别盛①干燥纯净的氨气、②二氧化氮与氧气的混合气(体积比:V(NO2 ):V(O2 )=4:1)、③一半空气的氯化氢,将它们分别倒置于盛足量水的水槽中,当水进入烧瓶中,并使气体充分溶解,假定烧瓶中溶液无损失,所得溶液的物质的量浓度之比为
A. 5:4:5 B. 1:1:1 C. 15: 12: 10 D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某物质灼烧时焰色反应为黄色,则下列判断正确的是( )
A.该物质一定是金属钠B.该物质一定是氯化钠
C.该物质一定是钠的化合物D.该物质一定含钠元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.某同学利用下列实验探究金属铝与铜盐溶液反应:

下列说法正确的是
A. 由实验1可以得出结论:金属铝的活泼性弱于金属铜
B. 溶液中阴离子种类不同是导致实验1、2出现不同现象的原因
C. 实验2中生成红色物质的离子方程式:Al+Cu2+→Al3++Cu
D. 由上述实验可推知:用砂纸打磨后的铝片分别与c(H+)均为0.2 mol/L的盐酸和硫酸反应,后者更剧烈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D,E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是
A. BADCE B. ECDBA C. ABCDE D. CDABE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝硅合金材料性能优良。铝土矿(含30% SiO2、40. 8% Al2O3和少量Fe2O3等)
干法制取该合金的工艺如下:
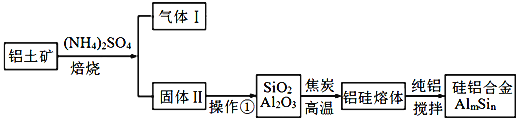
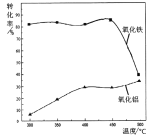
(1)焙烧除铁反应:4(NH4)2SO4+Fe2O3![]() 2NH4Fe(SO4)2+3H2O+6NH3(少部分Al2 O3发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如下图,最适宜焙烧温度为______________。指出气体I的用途 ____________(任写一种)。
2NH4Fe(SO4)2+3H2O+6NH3(少部分Al2 O3发生类似反应)。氧化物转化为硫酸盐的百分率与温度的关系如下图,最适宜焙烧温度为______________。指出气体I的用途 ____________(任写一种)。
(2)操作①包括:加水溶解、 过滤_______、_________。若所得溶液中加入过量NaOH溶液,含铝微粒发生反应的离子方程式为____________________
(3)用焦炭还原SiO2发生反应的化学方程式为_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一份澄清溶液, 可能含有 Na+、 K+、 NH4+、 Ca2+、 Fe3+、 SO42-、 CO32-、 SO32-、 Cl-、I-中的若干种, 且离子的物质的量浓度均为 0.1 mol·L-1(不考虑水解和水的电离)。 往该溶液中加入过量的盐酸酸化的 BaCl2 溶液, 无沉淀生成。 另取少量原溶液, 设计并完成如下实验:
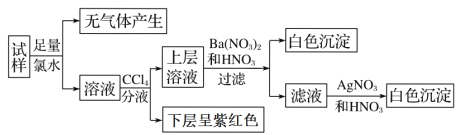
则关于原溶液的判断中不正确的是
A. 是否存在 Na+、K+需要通过焰色反应来确定
B. 通过CCl4 层的颜色变化,也能判断出原溶液中是否存在Fe3+
C. 虽然实验过程引入了氯元素, 但不影响原溶液是否存在Cl-的判断
D. 肯定不存在的离子是 Ca2+、Fe3+、SO42-、CO32-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com