
【题目】在一定条件下,固定容积的密闭容器中反应:2NO2(g)![]() O2(g)+2NO(g) ΔH>0,达到平衡。当改变其中一个条件X时,Y随X的变化符合图中曲线的是
O2(g)+2NO(g) ΔH>0,达到平衡。当改变其中一个条件X时,Y随X的变化符合图中曲线的是
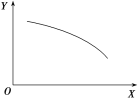
A. 当X表示温度时,Y表示O2的物质的量
B. 当X表示压强时,Y表示NO2的转化率
C. 当X表示反应时间时,Y表示混合气体的密度
D. 当X表示NO2的物质的量时,Y表示O2的物质的量
【答案】B
【解析】
由图象可以知道,随着X的增大,Y的值减小,
A.正反应吸热,升高温度,平衡向正反应方向移动;
B.从增大压强,平衡向逆反应方向移动分析;
C.达到平衡后,因混合气体的质量和体积不变,混合气体的密度不变;
D.增加NO2的物质的量时,平衡向正方向移动,氧气的物质的量增加。
A、反应吸热,升高温度,平衡向正反应方向移动,O2的物质的量增加,而图示曲线为减函数,故A错误;
B、增大压强,平衡向逆反应方向移动,NO2的转化率减小,故B正确;
C、达到平衡后,因混合气体的质量和体积不变,混合气体的密度不变,为定值,故C错误;
D、增加NO2的物质的量时,平衡向正方向移动,氧气的物质的量增加,故D错误;
综上所述,本题选B。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①2H2(g)+O2(g)=2H2O(l)ΔH=﹣570 kJ![]()
②2H2O(g)=2H2(g)+O2(g)ΔH=+483.6kJ![]()
③2C(s)+O2(g)=2CO(g)ΔH=﹣220.8 kJ![]()
④C(s)+O2(g)=CO2(g)ΔH=﹣393.5 kJ![]()
回答下列问题:
(1)上述反应中属于吸热反应的是_______(填写序号)。
(2)H2的燃烧热为________。
(3)燃烧10 g H2生成液态水,放出的热量为________。
(4)CO的燃烧热的热化学方程式为______________________。
(5)H2O(l)=H2O(g)ΔH=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关催化剂的催化机理等问题可从“乙醇催化氧化实验”得到一些认识,其实验装置如图所示。其实验操作为预先使棉花团浸透乙醇,并按照图示安装好装置;在铜丝的中间部分加热,片刻后开始(间歇性)鼓入空气,即可观察到明显的实验现象。
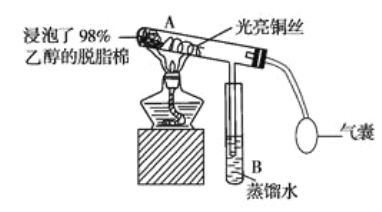
请回答以下问题:
(1)被加热的铜丝处发生反应的化学方程式为________________________________。
(2)从A管中可观察到____________的实验现象。从中可认识到在该实验过程中,催化剂参加了化学反应,还可认识到催化剂起催化作用时需要一定的_______________________。
(3)实验一段时间后,如果撤掉酒精灯,反应还能否继续进行?__________,原受热部分的铜丝有什么现象?____________,产生这种现象是因为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图所示(实线)。图中数据a(1,6)表示:在1 min时H2的物质的量是6mol。
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图所示(实线)。图中数据a(1,6)表示:在1 min时H2的物质的量是6mol。
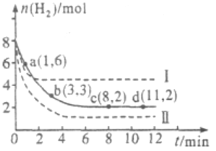
(1)a点正反应速率____(填“大于”“等于”或“小于”)逆反应速率。
(2)下列时间段平均反应速率最大的是____。
A.0~1 min B.1~3 min C.3~8 min D.8~11 min
(3)仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中所示(虚线)。曲线Ⅰ对应的实验条件改变是____,曲线Ⅱ对应的实验条件改变是______,体积不变再充入3 mol CO2和4 mol H2,达到新的平衡时,H2O(g)的体积分数____(填“增大”“不变”或“减小”)。
(4)若将1 mol CO2和3 mol H2充入该容器中,充分反应达到平衡后,若CO2转化率为a,则容器内的压强与起始压强之比为______(用a表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别将2mol SO2和1mol O2充入10L的容器中使之发生反应:2SO2+O2![]() 2SO3,并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变。若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3,并达到平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变。若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
A. 等于p% B. 大于p% C. 小于p% D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾[KA1(SO4)2·12H2O]是一种复盐,在造纸等方面应用广泛。采用废易拉罐制备明矾的过程如下图所示。
下列叙述错误的是
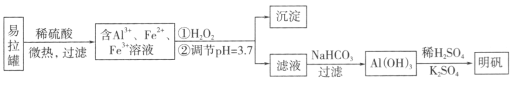
A. 合理处理易拉罐有利于环境保护和资源再利用
B. 从易拉罐中可回收的金属元素有Al、Fe
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用NaHSO4代替NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL 0.5 mol·L-1的稀硫酸。可供选择的仪器如下图
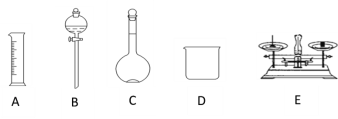
请回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是___________(填序号),配制上述溶液还需用到的玻璃仪器是_______________(填仪器名称)。
(2)使用容量瓶之前必须进行的操作是______________________________。
(3)经计算,需浓硫酸的体积为_____mL(小数点后保留 1位小数)。现有 ①10 mL
②50 mL ③100 mL三种规格的量筒,你选用的量筒是____(填序号)。
(4)配制溶液时,一般可分为以下几个步骤:
①量取 ②计算 ③稀释 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 其正确的操作顺序为:②→①→③→_________(填序号)。
(5)在配制过程中,其他操作都准确,下列操作使所配溶液浓度偏高的是_______ (填序号)
①洗涤量取浓硫酸的量筒,并将洗涤液转移到容量瓶中
②稀释后的硫酸溶液未等冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑤定容时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在药物制剂中,抗氧剂与被保护的药物在与O2发生反应时具有竞争性,抗氧性强弱主要取决于其氧化反应的速率。Na2SO3、NaHSO3和Na2S2O5是三种常用的抗氧剂。
已知:Na2S2O5 溶于水发生反应:S2O52+H2O=2HSO3
实验用品 | 实验操作和现象 |
①1.00×10-2mol/L Na2SO3溶液 ②1.00×10-2mol/L NaHSO3溶液 ③5.00×10-3mol/L Na2S2O5溶液 | 实验1:溶液①使紫色石蕊溶液变蓝,溶液②使之变红。 实验2:溶液①与O2反应,保持体系中O2浓度不变,不同pH条件下,c(SO32) 随反应时间变化如下图所示。 实验3:调溶液①②③的pH相同,保持体系中O2浓度不变,测得三者与O2的反应速率相同。 |
下列说法中,不正确的是

A. Na2SO3溶液显碱性,原因是:SO32+H2O![]() HSO3+OH
HSO3+OH
B. NaHSO3溶液中HSO3的电离程度大于水解程度
C. 实验2说明,Na2SO3在pH=4.0时抗氧性最强
D. 实验3中,三种溶液在pH相同时起抗氧作用的微粒种类和浓度相同,因此反应速率相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com