
����Ŀ�����ϱ�����MnO2��Fe3+��H2O2�Ʊ�O2�����д����á�ij����С��ͬѧ��ʵ���ҽ�������֤���鲢�о���H2O2�������ʡ��ش��������⣺
��1��������֧�ֱ�ʢ��2 mL10% H2O2��Һ���Թܣ���ͬѧ�ڵ�һ���ڶ�֧�Թ��зֱ����MnO2������FeCl3��Һ�����־��д����������ɣ������֧�Թ��м���������������Һ���۲�������Ŀ����________��
��2����ͬѧ����������ϣ���ô���������ͼ��ʾ��
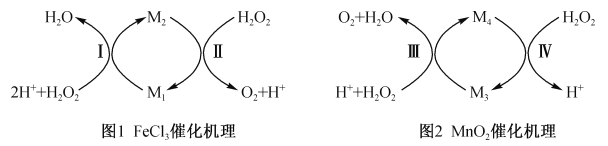
��ͼ1����M1��_______���ѧʽ����
��ͼ2����M4ΪMn2+����Ӧ�������ӷ���ʽΪ_____________��
��3����ͬѧ���Թ��м���2 ml. 3%��H2O2��Һ��0.5mL���ѣ�l mL1 mol/LH2SO4��Һ��3��4��0.5mol/L��K2Cr2O7��Һ�������ϲ��л���Ϊ��ɫ��CrO5��������Һ�����²�ˮ��Ϊ��ɫ��
�����ѳ���ΪCrO5���ȶ����⣬��һ������____________��
��һ��ʱ�����ɫ��ȥ������������������ͬʱˮ������Һ��Ϊ��ɫ����Cr3+������ɫ��Ӧ�����ӷ���ʽΪ________________��
���𰸡� ��֤FeCl3��Һ��ֻ��Fe3+���д����ã���Cl-û�� Fe2+ MnO2 +H2O2 +2 H+ =Mn2+ +O2��+2 H2O ��ȡCrO5 4CrO5 +12 H+=4Cr3++ 7O2��+6 H2O
����������1����Ϊ�Ȼ�����Һ���������Ӻ������ӣ����ݿ��Ʊ���������˵�����ʵ����Ϊ�Ա�ʵ�飬��Ŀ������֤FeCl3��Һ��ֻ��Fe3+���д����ã���Cl-û�С�
��2������ͼ1��֪��M1���Ա�˫��ˮ����ΪM2��M2����˫��ˮ����Ϊ����������M1���л�ԭ�ԡ�M2���������ԣ�����ͼ1����M1��Fe2+��
��ͼ2����M4ΪMn2+����Ӧ������ӷ���ʽΪMnO2 +H2O2 +2 H+ =Mn2+ +O2��+2 H2O��
��3����ͬѧ���Թ��м���2 ml. 3%��H2O2��Һ��0.5mL���ѣ�l mL1 mol/LH2SO4��Һ��3��4��0.5mol/L��K2Cr2O7��Һ�������ϲ��л���Ϊ��ɫ��CrO5��������Һ�����²�ˮ��Ϊ��ɫ��
�����ѳ���ΪCrO5���ȶ����⣬��һ����������ȡ������ȡCrO5 ��
��һ��ʱ�����ɫ��ȥ������������������ͬʱˮ������Һ��Ϊ��ɫ����Cr3+�������ݸ��Ļ��ϼ۽��ͣ������жϻ��ϼ����ߵ�Ԫ�����������Բ���������������������ɫ��Ӧ�����ӷ���ʽΪ4CrO5 +12 H+=4Cr3++ 7O2��+6 H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǻ�����������Ҫ��Ʒ�����������������Ϊ����һ�����ҹ�ҵ��չˮƽ�ı�־�������������Ҫ��ӦΪ��SO2(g)+ 1/2O2(g) ![]() SO3(g)��
SO3(g)��
��1�����º�ѹ�£�ƽ����ϵ��SO3�����������y��SO2��O2�����ʵ���֮�ȵĹ�ϵ��ͼ1����b��n(SO2)/n(O2)=________________��yΪ_____________(����)��

A��ƽ�ⳣ��
B��SO3��ƽ�����
C��O2��ƽ��ת����
D��SO2��ƽ��ת����
��2��Kp���Ը�����ƽ���ѹ����Ũ��ƽ�ⳣ��Kc�и������Ũ�ȵ�ƽ�ⳣ������400~650��ʱ��Kp���¶�(T /K)�Ĺ�ϵΪlgKp= - 4.6455�����ڴ�������SO2ת��ΪSO3��Ӧ����H_______(����>0������<0��)��
��3���ٸ÷�Ӧ�Ĵ���ΪV2O5�������Ӧ����Ϊ��
SO2+V2O5![]() SO3+V2O4 K1 1/2O2+V2O4
SO3+V2O4 K1 1/2O2+V2O4![]() V2O5 K2
V2O5 K2
������ͬ�¶���2SO2(g)+O2(g) ![]() 2SO3(g)��ƽ�ⳣ��K=____________(�Ժ�K1��K2�Ĵ���ʽ��ʾ)��
2SO3(g)��ƽ�ⳣ��K=____________(�Ժ�K1��K2�Ĵ���ʽ��ʾ)��
��V2O5�ӿ췴Ӧ���ʵ�ԭ����_____________________________��
��4����7.0% SO2��11% O2��82% N2(��ֵ��Ϊ�����������)ʱ��SO2ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ2������ʽ����460����1.0 atm�£�SO2(g)+1/2 O2(g) ![]() SO3(g)��Kp=_______(��֪��������ķ�ѹ=��ѹ����������������)��
SO3(g)��Kp=_______(��֪��������ķ�ѹ=��ѹ����������������)��

��5���ۺϵڣ�4����ͼ����Ϣ����ҵ����ѹǿͨ�����ó�ѹ��ԭ����__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2014��5��21�գ��ж�ǩ����30����Ȼ����Ӧ��ͬ����Ϊ�ҹ��õ������Դ����Ҫ��Դ����Ȼ������Ҫ�ɷ���
A. CH4 B. CO2 C. CO D. H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������100mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ������ѻ���ɱ�״̬����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL�� | 50 | 120 | 232 | 290 | 310 |
��1����һʱ��Σ�ָ0��1��1��2��2��3��3��4��4��5min����Ӧ�������
��2����һ��ʱ�εķ�Ӧ������С ��
��3����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ���ʣ�����Һ������䣩 ��
��4�������Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ������������������������зֱ����������������Һ��
A.����ˮ
B.NaCl��Һ
C.Na2CO3��Һ
D.CuSO4��Һ
����Ϊ���е��ǣ����ţ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ӦNa2CO3+2HCl��2NaCl+H2O+CO2�������ӷ���ʽ��
A. CO32-+2H+��H2O+CO2��
B. CO32-+H+��H2O+CO2��
C. CO32-+2HCl��2Cl-+H2O+CO2��
D. Na2CO3+2H+��2Na++H2O+CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¶��£���2 mol SO2��1mol O2����10 L�����ܱ������У�������Ӧ2SO2(g) +O2(g)![]() 2SO3(g) ��H =-196 kJ mol-1��5 minʱ�ﵽƽ�⣬��÷�Ӧ����166. 6 kJ������˵���������
2SO3(g) ��H =-196 kJ mol-1��5 minʱ�ﵽƽ�⣬��÷�Ӧ����166. 6 kJ������˵���������
A. 0��5 min�ڣ���O2��ʾ��ƽ����Ӧ����V(O2)=0.017 mol��L-1��min-1
B. ![]() ��ֵ����ʱ���÷�Ӧ�ﵽƽ��״̬
��ֵ����ʱ���÷�Ӧ�ﵽƽ��״̬
C. ������O2��Ũ�ȣ�SO2��ת��������
D. �������䣬����ʼʱ����4 mol SO2��2 mol O2��ƽ��ʱ�ų�������С��333.2 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ�����ʽ���ֶ���������ͼ������Ԫ�����ڱ���һ���֣�1��36��Ԫ�أ����Ա���ѧ����Ԫ�����ڱ���˼������Ԫ�����ڱ��������ɣ�����˵����ȷ���ǣ� �� 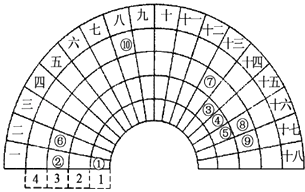
A.�ڡ��ࡢ���Ӧ�����Ӱ뾶���μ�С
B.�ݵ����ֺ��ػ�ѧ���ʲ�ͬ
C.Ԫ��=10 ��ڳ������ڱ��������ڵ�VIIIB��
D.�ܵ�����������Ӧ��ˮ�����������⻯�ﷴӦ���������ӻ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com