
| ��� | NaOH/mol•L-1 | HA/mol•L-1 | �����Һ��pH |
| �� | 0.1 | 0.1 | pH=9 |
| �� | c | 0.2 | pH=7 |
| �� | 0.1 | 0.2 | pH��7 |
���� ��1��������ʵĵ����ǿ���ģ�������ȫ���룻������������Ȱ�һС��pH��ֽ���ڱ��������Ƭ�ϣ����ò�����պԦ��Һ������ֽ���в�������ɫ�������ɫ���Ա�ȷ����Һ��pH��
��2����ȷȡpH=1��HA��Һ��ϡ�����10.00mL������ʽ�ζ��ܣ�pH��Ϊ1��HA��Һ��ϡ�����У�˵��������Ũ����ȣ�����ˮ�����ӻ����õ�����������Ũ����ȣ�����������Һ��ˮ�Ķ����̶���ͬ��
��3��������ˮ��Һ�ﲿ�ֵ��룬����������Ũ��С����Ũ�ȣ����п��Ӧʱ������������Ӧ���ʺ�������Ũ�ȳ����ȣ��������������ķ�Ӧ����ȷ�����ǿ����
��4������Ϊǿ�ᣬ�������Ũ�Ȼ��ʱpH=7����HAΪ���ᣬ�������Ũ�Ȼ����Һ��pH����7����Ϊ��֤pH=7��Ӧʹ��Ũ�ȴ���0.1mol/L������ϵ���غ��������Ũ�ȹ�ϵ��
��5���ɢ���ʵ������֪����Ϻ�ΪHA��NaA�Ļ��Һ��pH=7����ĵ�������ε�ˮ�⣮
��� �⣺��1�����������ˮ��Һ�в��ֵ��룬��HAΪ���ᣬ0.1 mol/L HA��Һ��c��H+����0.1 mol/L����Һ��pH��1���ײⶨ��ҺPH�ľ�������������Ȱ�һС��pH��ֽ���ڱ��������Ƭ�ϣ����ò�����պԦ��Һ������ֽ���в�������ɫ�������ɫ���Ա�ȷ����Һ��pH��
�ʴ�Ϊ�������Ȱ�һС��pH��ֽ���ڱ��������Ƭ�ϣ����ò�����պԦ��Һ������ֽ���в�������ɫ�������ɫ���Ա�ȷ����Һ��pH��
��2�����ҵķ����ĵڢٲ��У�ȷ��ȡ10.00mL������Һ��Ҫ�õ��Ķ�����������ʽ�ζ��ܣ�pH��Ϊ1��HA��Һ��ϡ������������Ũ����ͬ������ˮ�ĵ���̶ȵ���ͬ��
�ʴ�Ϊ����ʽ�ζ��ܣ�c��
��3���������Խϡ����̶�Խ��ϡ����ͬ����������������Ũ�ȱ仯С��������Ũ�ȴ��ҵķ����У�˵��HA��������ʵ���Ҫ������װHA��Һ���Թ��зų�H2�����ʿ죬
�ʴ�Ϊ��B��
��4�����ķ�����ͨ����Ţٵ�����֤��HAΪ���ᣬ�����������Ũ�Ȼ����Һ�ʼ��ԣ���Ţ��г����ԣ�����c��0��l�����ݵ���غ㣬�û��Һ�е�����Ũ�ȣ�c��Na+��=c��A-����
�ʴ�Ϊ������=��
��5�����ķ����У���Ţ�ʵ�����ҺΪ��Ũ�ȵ�NaA��HA�Ļ��Һ��NaAˮ��ʼ��ԡ�HA��������ԣ�ʵ�����ݱ�����Һ�����ԣ������Һ��HA�ĵ���̶ȱ�NaA��ˮ��̶�ǿ���ʴ�Ϊ��ǿ��
���� ���⿼��������ʵĵ��룬Ϊ��Ƶ���㣬���ؿ���ѧ�������ж���������ȷ������ʵ����ص㼰������ʵ���Ӱ�������ǽⱾ��ؼ���ע�⣺��Ӱ��ˮ����̶���������Ũ���йء������ǿ���أ�Ϊ�״��㣮


 �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| c��I-��/mol•L-1 | c��Fe3+��/mol•L-1 | v/mol•L-1•s-1 | |
| �� | 0.20 | 0.80 | 0.032k |
| �� | 0.60 | 0.40 | 0.144k |
| �� | 0.80 | 0.20 | 0.128k |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
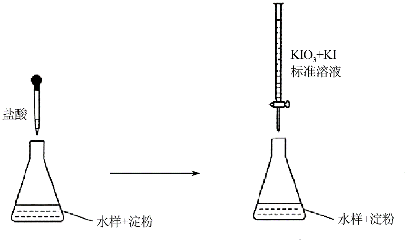
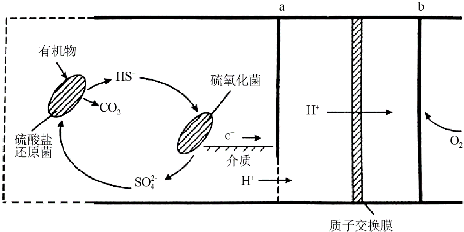
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
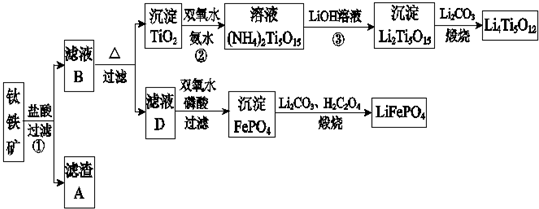
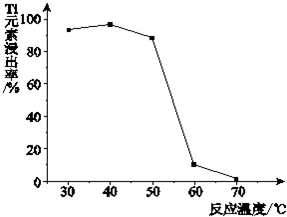
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�2.24L����������������Ӧ��ת�Ƶ�����Ϊ0.2NA | |
| B�� | ��״���£�2.24L NO2������������Ϊ3.9 NA | |
| C�� | 7.8gNa2S��Na2O2�Ļ�����к��е���������������0.1 NA | |
| D�� | ���³�ѹ�£���0.1mol����ͨ��ˮ�з�����ѧ��Ӧ��ת�Ƶ�����Ϊ0.1 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2KBr+Cl2=2KCl+Br2 | B�� | CaCO3=CaO+CO2�� | ||
| C�� | SO3+H2O=H2SO4 | D�� | MgCl2+2NaOH=Mg��OH��2��+NaCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ú�����������Ȼ����ʯ�����л������� | |
| B�� | ���û�ʯȼ��ȼ�շų�������ʹ�ֽ���������������ܿ������о����� | |
| C�� | ��ѧ��Դ�ŵ硢ֲ�������ö��ܷ�����ѧ�仯��������������ת�� | |
| D�� | ����ѧ�����жϿ���ѧ���ų������������γɻ�ѧ�������յ���������Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҵ������������ˮ�ࡢƯ�۾���Ҫ��ʯ��ʯΪԭ�� | |
| B�� | �û���̿Ϊ�ǽ���ɫ���ô�������Ư��ֽ����ԭ����ͬ | |
| C�� | ����ӻ�������֬��������ˮ��Ϊ��������͵�С���Ӳ��ܱ����� | |
| D�� | ˾ĸ�춦����Զ���װ塢�л�������ԭ�������ںϽ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com