

科目:高中化学 来源: 题型:
已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
A.-44.2kJ·mol-1 B.+44.2 kJ·mol-1 C.-330 kJ·mol-1 D.+330 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省忻州一中高二上学期期末联考化学(理)试卷(A)(带解析) 题型:单选题
已知H2(g)+Cl2(g)="2HCl(g)" △H =" ―184.6" kJ·mol-1,下列说法中正确的是
| A.该反应为吸热反应 |
| B.H2的能量一定高于HCl |
C.反应HCl(g)=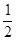 H2(g)+ H2(g)+ 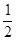 Cl2(g) 的 △H为 +92.3 kJ·mol-1 Cl2(g) 的 △H为 +92.3 kJ·mol-1 |
| D.该反应为放热反应,故不必加热就可发生反应 |
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高二上学期期末考试化学试卷(解析版) 题型:填空题
利用太阳能分解水生成的氢气,在催化剂作用下氢气与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热ΔH分别为-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
(1)用太阳能分解10 mol水消耗的能量是 kJ。
(2)液态甲醇不完全燃烧生成一氧化碳气体和液态水的热化学方程式为 。
(3)
在容积为2 L的密闭容器中,由CO2和H2合成甲醇,反应式:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):
CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):
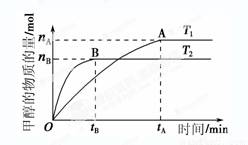
①可逆反应的平衡常数表达式K=
②下列说法正确的是
A.温度为T1时,从反应开始到平衡,生成甲醇
的平均速率为v(CH3OH)= mol·L-1·min-1
mol·L-1·min-1
B.该反应在T1时的平衡常数比T2时的小
C.该反应为放热反应
D.处于A点的反应体系从T1变到T2,达到平衡时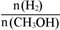 增大
增大
③在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为 ;
(4) 在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,总反应式为
2CH3OH + 3O2=2CO2+4H2O,则正极的反应式为 ;
负极的反应式为 。[来
查看答案和解析>>
科目:高中化学 来源:2014届山西省高二上学期期末联考化学(理)试卷(A)(解析版) 题型:选择题
已知H2(g)+Cl2(g)="2HCl(g)" △H =" ―184.6" kJ·mol-1,下列说法中正确的是
A.该反应为吸热反应
B.H2的能量一定高于HCl
C.反应HCl(g)=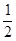 H2(g)+
H2(g)+
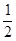 Cl2(g) 的 △H为 +92.3 kJ·mol-1
Cl2(g) 的 △H为 +92.3 kJ·mol-1
D.该反应为放热反应,故不必加热就可发生反应
查看答案和解析>>
科目:高中化学 来源:2013届吉林省高二上学期期末考试化学试卷 题型:选择题
已知H2(g) + Cl2(g) = 2HCl(g) △H= ―184.6kJ·mol-1, 则反应HCl(g) =1/2H2(g) + 1/2Cl2(g)的△H为
A、+184.6kJ·mol-1 B、―92.3kJ·mol-1 C、+92.3kJ D、+92.3 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com