
12分)某学生用0.1000mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如
下几步:
A 移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
B 用标准溶液润洗滴定管2-3次
C 把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
E.调节液面至0或0刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面刻度
(1) 正确操作的顺序是(用序号字母填写) B- 。
(2) 滴定开始后,眼睛注视 ,判断滴定终点的现象是:
(3) 下列操作中可能使所测盐酸的浓度数值偏高的是
A 碱式滴定管未用标准溶液润洗就直接注入标准液
B 滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留
C 碱式滴定管在滴定前有气泡,滴定后气泡消失
D 读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数
(4)滴定开始和结束时,碱式滴定管中的液面如图C所示,则终点读数为 mL,所测盐酸溶液的浓度为 mol/L。
26. (12分) (1) DCEAF (2分) (2) 锥形瓶内溶液颜色的变化(2分)
溶液由无色变为(浅)红色,且半分钟内溶液颜色不发生改变(2分,每点1分)
(3) AC(2分,选1个正确给1分,有错不给分) (4)25.90(2分) 0.1295 mol/L(2分)
解析试题分析:(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,所以正确的顺序为BDCEAF;(2) 滴定开始后,两眼应该注视锥形瓶内溶液的颜色变化;滴定时,锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色,可说明达到滴定终点:(3)碱式滴定管未用标准溶液润洗就直接注入标准液,会导致标准液稀释,根据c(待测)=C(标)xV(标)/V(待)分析,可得c(待测)偏高,A偏高;滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留,没有影响HCl的物质的量,B无影响;碱式滴定管在滴定前有气泡,滴定后气泡消失,会导致末读数据增大,结果偏高,C偏高;读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数,开始读数偏大,结束读数偏小,结果偏小,D错误,下列操作中可能使所测盐酸的浓度数值偏高的是A、C(4)滴定管的0刻度在上,1cm之间有10个间隔,所以终点读数为25.90mL,根据c(待测)=C(标)xV(标)/V(待)计算可得所测盐酸溶液的浓度为0.1295 mol/L。
考点:考查中和滴定等知识。


科目:高中化学 来源:2013-2014广西桂林市、崇左市、防城港市、北海市高三化学试卷(解析版) 题型:选择题
下列表述正确的是
A、碳酸氢根离子的电离方程式可表示为:HCO3-+H2O H3O++CO32-
H3O++CO32-
B、酸性条件下,KIO3溶液与KI溶液反应生成I2的离子方程式为:IO3-+5I-+3H2O=I2+6OH-
C、氯气具有酸性,可与烧碱溶液或石灰乳反应制备含氯消毒剂
D、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
“化学是一门中心学科,与社会、生活、科研密切的关系”。下列叙述中,不正确的是
| A.大量使用燃煤发电是形成雾霾的主要原因 |
| B.天然气、煤气大量泄漏遇到明火会爆炸 |
| C.利用化学反应可实现12C到14C的转化 |
| D.晶体硅可用于光伏发电、制造芯片 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(10分)某实验小组用0.50 mol·L-1NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol·L-1NaOH溶液
(1)若实验中大约要使用470 mL NaOH溶液,至少需要称量NaOH固体 g。
(2)从图中选择称量NaOH固体所需要的仪器是(填字母): 。
| 名称 | 托盘天平 | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
| 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应中,在高温下不能自发进行的是( )
A.CO(g) C(s)+O2(g) C(s)+O2(g) |
B.NH4Cl(s) NH3(g)↑+HCl(g)↑ NH3(g)↑+HCl(g)↑ |
C.(NH4)2CO3(s) NH4HCO3(s)+NH3(g) NH4HCO3(s)+NH3(g) |
D.MgCO3(s) MgO(s)+CO2(g) MgO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 下列说法中不正确的是
下列说法中不正确的是
A.高吸水性树脂属于功能高分子材料
B.SiC、Al2O3的熔点很高,可用作高温结构陶瓷
C.光导纤维、合成纤维和人造纤维都是有机高分子化合物
D.合金拓展了金属材料的使用范围,合金中也可能含有非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
有关物质间有下图所示的转化关系。其中:A的浓溶液与单质B在加热时才发生反应①;A的稀溶液与足量B发生反应②。据此填写下列空白: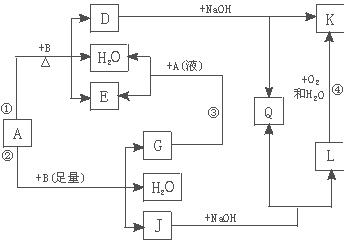
(1)反应④的现象是 。
(2)写出反应②的离子方程式 。
(3)根据题示信息判断,A的浓溶液和单质B加热时能否产生G,说明理由(写出化学方程式回答):
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z原子与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_____、_______;杂化轨道分别是________、_________;a分子的立体结构是____________;
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______晶体、_______晶体;
(3)X的氧化物与Y的氢化物中,分子极性较小的是(填分子式) ;
(4)Y与Z比较,电负性较大的是____________;
(5)W的元素符号是 ,其+2价离子的核外电子排布式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com