
| A. | 20℃时,铝的密度为2.7 g/cm3,则1个Al原子的体积为($\frac{10}{{N}_{A}}$)cm3 | |
| B. | 25℃、101KPa下,16 g O2与O3的混合气体中含电子数为8NA | |
| C. | 25℃、101KPa下,11.2L Cl2含有的分子数小于0.5NA | |
| D. | 0℃、101KPa下,等体积的CH4和CCl4中含C原子数相等 |
分析 A、求出1mol铝的质量和体积,然后根据1mol铝中含NA个铝原子来分析;
B、氧气和臭氧均由氧原子构成;
C、25℃、101KPa下,气体摩尔体积大于22.4L/mol;
D、0℃、101KPa下,四氯化碳为液体.
解答 解:A、1mol铝即NA个铝原子的质量为27g,体积为$\frac{27g}{2.7g/mL}$,则1个Al原子的体积为$\frac{10}{{N}_{A}}$cm3,故A正确;
B、氧气和臭氧均由氧原子构成,故16g氧气和臭氧的混合物中含有的氧原子的物质的量为1mol,而1mol氧原子的核外有8mol电子,故含8NA个电子,故B正确;
C、25℃、101KPa下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,则分子个数小于0.5NA个,故C正确;
D、0℃、101KPa下,四氯化碳为液体,而甲烷为液体,故两者的物质的量不同,则含有的碳原子个数不同,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


科目:高中化学 来源: 题型:选择题
| A. | 石油裂解的目的是提高汽油等轻质油的产量和质量 | |
| B. | “神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 | |
| C. | 补血口服液中添加维生素c,作为氧化剂 | |
| D. | 用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氰、硫、碳的氧化物有多种,其中S02和N0x都是大气污染物,对它们的研究有助于空气的净化.
氰、硫、碳的氧化物有多种,其中S02和N0x都是大气污染物,对它们的研究有助于空气的净化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石膏:CaSO4•2H2O,可用于制造各种模型 | |
| B. | 重晶石:BaCO3,可作白色颜料、医疗上“钡餐” | |
| C. | 绿矾:FeSO4•7H2O,可生产净水剂、防止缺铁性贫血的药剂 | |
| D. | 胆矾:CuSO4•5H2O,可用于生产农药 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
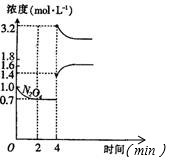
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:K+ CH3COO- SO42- Na+ | |
| B. | 含有0.1mol/LCa2+的溶液中:Na+SO42- K+ Cl- | |
| C. | 含有0.1mol/LMg2+的溶液中:Na+SO42- K+ HCO3- | |
| D. | 滴入酚酞显红色的溶液:K+ HCO3-Ba2+Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+、NH4+、Fe3+、Ba2+ |
| 阴离子 | Cl-、CO32-、HCO3-、SO42- |
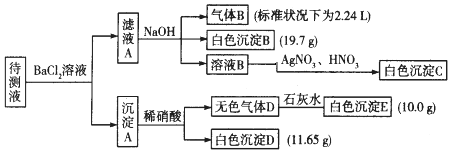
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3-->Al(OH)3 | B. | Cu-->CuCl2 | C. | Fe-->FeCl2 | D. | Na-->NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com