
 nC(g)+2D(g) 5 s后反应达到平衡状态,生成2 mol D,经测定以C表示的平均反应速率为0.1 mol·L-1·s-1。则下列结论中正确的是
nC(g)+2D(g) 5 s后反应达到平衡状态,生成2 mol D,经测定以C表示的平均反应速率为0.1 mol·L-1·s-1。则下列结论中正确的是| A.以A表示的平均反应速率为0.1 mol·L-1·s-1 |
| B.平衡时,B的浓度为1 mol·L-1 |
| C.n值等于1 |
| D.平衡时B的转化率为50% |
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源:不详 题型:单选题
 后测得密闭容器内的压强是起始时的0.9倍,在此时间内
后测得密闭容器内的压强是起始时的0.9倍,在此时间内 是
是A. | B.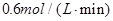 |
C. | D. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) ΔH = -92.2kJ?mol—1,测得0到10秒内,c(H2)减小了0.75mol?L—1,下列说法正确的是
2NH3(g) ΔH = -92.2kJ?mol—1,测得0到10秒内,c(H2)减小了0.75mol?L—1,下列说法正确的是| A.10到15秒内c(NH3) 增加量等于0.25mol ?L—1 |
| B.10秒内氨气的平均反应速率为0.025mol?L—1·s—1 |
| C.达平衡后,分离出少量NH3,v正增大 |
| D.该反应的逆反应的活化能不小于92.2kJ?mol—1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 的容器中进行,8分钟消耗反应物
的容器中进行,8分钟消耗反应物 。在另一条件下,该气体在
。在另一条件下,该气体在 容器中发生分解,10分钟内消耗反应物10g。在这两种情况下,平均反应速率之比为 。
容器中发生分解,10分钟内消耗反应物10g。在这两种情况下,平均反应速率之比为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
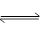 2NH3反应中,自反应开始至2 s末,氨的浓度由0变为0.4 mol·L-1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
2NH3反应中,自反应开始至2 s末,氨的浓度由0变为0.4 mol·L-1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )| A.0.3 mol·L-1·s-1 | B.0.4 mol·L-1·s-1 |
| C.0.6 mol·L-1·s-1 | D.0.8 mol·L-1·s-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
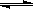 2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的平均速率v为( )
2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的平均速率v为( )| A.v(X)=0.05mol·L-1·min-1 | B.v(Z)= 0.10mol·L-1·min-1 |
| C.v(Y)=0.10mol·L-1·min-1 | D.v(W)=0.05mol·L-1·s-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增大压强,活化分子百分数增大,化学反应速率一定增大 |
| B.增大浓度,活化分子百分数增大,化学反应速率一定增大 |
| C.加入反应物,使活化分子百分数增大,化学反应速率增大 |
| D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,增大化学反应速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学反应速率是衡量化学反应进行快慢程度的物理量 |
| B.化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示 |
| C.在同一个反应中,各物质的反应速率之比等于化学方程式中的计量数之比 |
| D.化学反应速率的常用单位有mol/(L·s)和mol/(L·min) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.前2秒,以N2O4的浓度变化表示的平均反应速度为0.01摩/升·秒 |
| B.在2秒时体系内压强为开始时压强的1.1倍 |
| C.在平衡体系内含N2O40.25摩 |
| D.平衡时, N2O4的转化率为40% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com