
分析 根据B离子被还原时获得电子数计算B离子化合价,根据生成氢气利用电子转移守恒计算B的物质的量,再根据M=$\frac{m}{n}$计算计算B的相对原子质量.
解答 解:当B元素的离子$\frac{1}{3}$摩尔被还原时需得到6.02×1023个电子,即需要1mol电子,则B离子化合价为$\frac{1mol}{\frac{1}{3}mol}$=+3,1.2g氢气物质的量为$\frac{1.2g}{2g/mol}$=0.6mol,由电子转移守恒可知10.8gB的物质的量为$\frac{0.6mol×2}{3}$=0.4mol,B的摩尔质量为$\frac{10.8g}{0.4mol}$=27g/mol,故B的相对原子质量为27,
答:B的相对原子质量为27.
点评 本题考查氧化还原反应计算,关键是电子转移守恒的应用,较好的考查学生分析计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,若物质物质的量相等,其体积一定相等 | |
| B. | 1升氮气比1升氧气的质量小 | |
| C. | 等体积的二氧化碳和一氧化碳所含分子数一定相等 | |
| D. | 相同条件下的一氧化碳和氮气,若体积相等,则质量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2比O3稳定,由O2变O3为放热反应 | |
| B. | O3比O2稳定,由O2变O3为吸热反应 | |
| C. | 等质量的O2比O3能量低,由O2变O3为吸热反应 | |
| D. | 等质量的O2比O3能量高,由O2变O3为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,气体颜色加深,则此反应为吸热反应 | |
| B. | 慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅 | |
| C. | 慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍 | |
| D. | 恒温恒容时,充入NO2气体,平衡向右移动,NO2的转化率增大,混合气体的颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.00mol NH4Cl中含有6.02×1023个NH4Cl分子 | |
| B. | 1.00mol NH4Cl中,${NH}_{4}^{+}$的数目为6.02×1023 | |
| C. | 欲配制1.00L 1.00mol•L-1NH4CL的溶液,可将53.5gNH4Cl溶于1.00L水中 | |
| D. | 1.00L 1.00mol•L-1 NH4Cl溶液中含有6.02×1023个NH3分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g NaCl | B. | 10g NaOH固体 | C. | 10g BaSO4固体 | D. | 10g AgNO3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
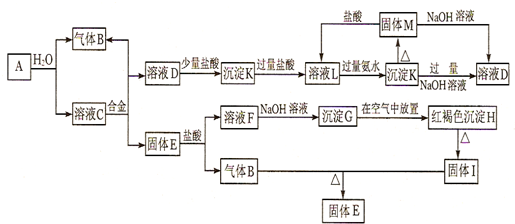
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com