
| A. | ${\;}_{a}^{b}$R | B. | ${\;}_{a+2}^{a+b+2}$R | C. | ${\;}_{a-2}^{a+b}$R | D. | ${\;}_{a+2}^{a+b+2}$R |
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:选择题
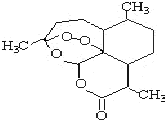 青蒿素是一种由青蒿中分离得到的具有新型化学结构的抗疟药,结构如图所示.有关该化合物的叙述正确的是( )
青蒿素是一种由青蒿中分离得到的具有新型化学结构的抗疟药,结构如图所示.有关该化合物的叙述正确的是( )| A. | 分子式为:C16H20O5 | |
| B. | 该化合物在一定条件下不能与NaOH溶液反应 | |
| C. | 青蒿素与维生素一样是水溶性的 | |
| D. | 该化合物中含有过氧键,一定条件下有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都由C和H两种元素组成的饱和烃 | |
| B. | 都能使酸性KMnO4溶液褪色 | |
| C. | 都能发生加成反应和取代反应 | |
| D. | 在氧气中完全燃烧后都生成CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
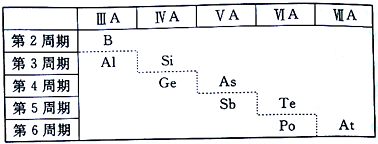
| A. | 虚线右上方的元素为金属元素 | |
| B. | 第6周期ⅤA族的元素为非金属元素 | |
| C. | 可在虚线附近寻找用于制造半导体材料的元素 | |
| D. | 可在虚线附近寻找稀土元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用浓硫酸可区分蛋白质溶液和淀粉溶液 | |
| B. | 在蛋白质溶液中滴加硫酸铜溶液,生成白色沉淀,加水后,沉淀溶解 | |
| C. | 皂化实验后期加入饱和食盐水使高级脂肪酸盐析出,浮在混合液上面,通过纱布可滤去水层 | |
| D. | 取淀粉水解液,加入新制Cu(OH)2浊液,加热,未见砖红色沉淀生成,说明淀粉尚未水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com