
| A. | 中子数为3的He原子:32He | B. | HCl的电子式: | ||
| C. | S2-的结构示意图: | D. | 肼(N2H4)的结构简式:H2N-NH2 |
分析 A.元素符号左上角表示质量数,左下角为质子数,中子数=质量数-质子数;
B.HCl分子是由1个氢原子和1个氯原子通过共用1对电子结合而成的共价化合物,无阴阳离子;
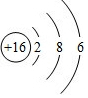
C.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,用小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数;
D.肼的分子式为N2H4,是氮原子和氢原子形成四个共价键,氮原子和氮原子之间形成一个共价键形成的共价化合物.
解答 解:A.中子数为3的He原子,质量数=2+3=5,符号为:52He,故A错误;
B.HCl分子是由1个氢原子和1个氯原子通过共用1对电子结合而成的共价化合物其电子式为 ,故B错误;
,故B错误;
C.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,硫离子结构示意图为 ,故C错误;
,故C错误;
D.肼的分子式为N2H4,是氮原子和氢原子形成四个共价键,氮原子和氮原子之间形成一个共价键形成的共价化合物,结构简式:H2N-NH2,故D正确;
故选D.
点评 本题考查常用化学用语正误判别,掌握相关用语的书写规范是解答关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①④⑤⑥ | C. | ②③④⑤ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4、CuO | B. | C、CuO | C. | Fe、MnO2 | D. | Si、FeS |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌片为正极 | |
| B. | 该电池工作时电能转化为化学能 | |
| C. | 该电池的总反应为Zn+2H+═Zn2++H2↑ | |
| D. | 电子由铜片通过导线流向锌片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L | B. | 0.2 mol/L | C. | 0.3 mo/L | D. | 0.4 mo/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠是一种淡黄色固体 | |
| B. | 过氧化钠可用于呼吸面具或潜水艇中作为氧气的来源 | |
| C. | 过氧化钠与水反应后的溶液滴加几滴酚酞溶液,溶液会变为红色 | |
| D. | 1mol过氧化钠与水反应可生成1mol氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY3 | B. | XY | C. | X3Y | D. | X2Y3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 I.(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.图中t1 时引起平衡移动的条件可能是增大压强.
I.(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.图中t1 时引起平衡移动的条件可能是增大压强.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com