
【题目】下列说法或有关化学用语的表达正确的是( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的外围电子排布图为: ![]()
C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】氢氟酸能腐蚀玻璃。25℃下,向20mL0.2molL-1的氢氟酸中滴加0.2molL-1的NaOH溶液时,溶液的pH变化如图所示。
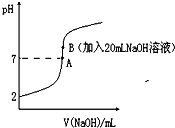
已知:电离度(α)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力。![]()
请回答下列问题:
(1)在氢氟酸的稀溶液中,通过改变以下条件能使氢氟酸的电离度[![]() (HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_____________。
(HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_____________。
a.升高温度 b.向溶液中滴入2滴浓盐酸 c.加入少量NaF固体 d.加水
(2)在此温度下,氢氟酸的电离平衡常数Ka(HF)为:_____,电离度α(HF)为______%。
(3)下列有关图中各点微粒浓度关系正确的是________。
a.在A处溶液中:c(F—)+c(HF)=0.2 molL-1
b.在B处溶液中:c(H+)+c(HF)= c(OH—)
c.在B处溶液中:c(Na+)>c(F—)>c(H+)>c(OH—)
d.在A和B处溶液中都符合:![]() = Ka(HF)
= Ka(HF)
(4)向此氢氟酸溶液中滴加10mlNaOH溶液后,请将HF分子与溶液中的离子浓度一起从大到小排序 ___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的制备与工业生产相符的是( ) ①NH3 ![]() NO
NO ![]() HNO3
HNO3
②浓HCl ![]() Cl2
Cl2 ![]() 漂白粉
漂白粉
③MgCl2(aq) ![]() 无水MgCl2
无水MgCl2 ![]() Mg
Mg
④饱和NaCl(aq) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
⑤铝土矿 ![]() NaAlO2溶液
NaAlO2溶液 ![]() Al(OH)3
Al(OH)3 ![]() Al2O3
Al2O3 ![]() Al.
Al.
A.①④⑤
B.①③⑤
C.②③④
D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途不具有对应关系的是 ( )
A. 常温下铁遇浓硫酸发生钝化,可用铁质容器贮运浓硫酸
B. 浓硫酸有吸水性,可用于干燥HCl气体
C. Na 2O2具有强氧化性,可作潜水艇里氧气的来源
D. 明矾溶于水可形成氢氧化铝胶体,可用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学欲除去固体氯化钠中混有的氯化钙,请根据如下实验方案回答问题. 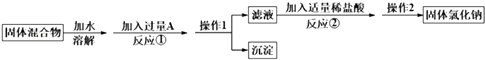
(1)A物质的化学式为;操作1的名称是 .
(2)反应①中加入略过量的A物质的目的是;判断A已过量的实验操作方法是 .
(3)写出反应②的化学方程式: . 如果加入盐酸过量,则对所得到的氯化钠的纯度(填“有”或“没有”)影响.
(4)实验时称取样品的质量为185.0g,经过操作1后,测得沉淀(不溶于水)的质量为50.0g,则样品中NaCl的质量分数是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科技、社会、环境密切相关,下列说法中不正确的是( )
A.单晶硅常用于制光导纤维
B.可用醋酸除去水瓶中的水垢
C.开发氢能源汽车,可减少PM2.5的排放
D.工业合成氨属于人工固氮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日前中国量子物质科学协同创新中心的江颖课题组和王恩哥课题组合作,在水科学领域取得重大突破,在国际上首次实现了水分子的亚分子级分辨成像,使得解析水的氢键网络构型成为可能.(图a是实验器件示意图,图b是拍摄到的图片的一部分,图c是图b所对应的结构示意图)下列有关说法不正确的是( ) 
A.图a所示实验器件中,用氯化钠作为绝缘薄膜层,是因为氯化钠晶体不导电
B.图b是表示一个H2O分子内部的氢键和氢氧共价键结构特征示意图
C.水分子间形成氢键使水的熔点和沸点升高
D.H2O分子的稳定性很强,是因为分子内氢氧共价键强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W,X,Y,Z的原子序数依次增大,W,X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性.下列说法正确的是( )
A.简单离子半径:W<X<Z
B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:W<Y
D.最高价氧化物的水化物的酸性:Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com