
 (2)S2-﹥O2-﹥Na+ (3)H++HSO3-=H2O+SO2 ↑
(2)S2-﹥O2-﹥Na+ (3)H++HSO3-=H2O+SO2 ↑


科目:高中化学 来源:不详 题型:单选题
| A.元素周期表中查得的相对原子质量为同位素的相对原子质量 |
| B.化学键的变化一定会引起化学反应的变化 |
| C.只含有共价键的物质一定是共价化合物 |
| D.全部由极性键构成的分子不一定是极性分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.元素铯的两种核素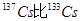 多4个质子 多4个质子 |
| B.P、S、C1得电子能力和最高价氧化物对应水化物的酸性均依次增强 |
| C.元素原子的最外层电子数越多,越容易得电子 |
| D.从上到下,第VIIA族元素氢化物的热稳定性和还原性均依次减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
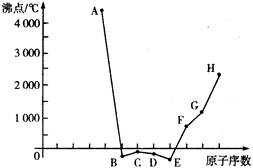
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知Sr元素位于第五周期IIA族,故Sr(OH)2碱性比Mg(OH)2弱 |
| B.己知As元素位于第四周期VA族,故NH3比 AsH3稳定 |
| C.元素周期表分为7个主族、7个副族、1个0族、1个VIII族,共18个纵行 |
| D.副族元素中没有非金属元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | | | ||||||
| | | | | | | A | B | |
| C | | | D | E | F | G] | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.热稳定性:H2O>HF>H2S | B.沸点:HF>HCl>HBr |
| C.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl | D.氧化性:Fe3+>Cu2+>H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com