
| A、向 苯粉钠溶液中通入少量的CO2:2C6H5O+CO2+H2O→2C6H5OH+CO32- | ||||
| B、铝溶于氢氧化钠溶液:Al+2OH-+H2O═AlO2-+2H2↑ | ||||
| C、NH4HSO4和过量的氧化钠溶液反应:NH4++OH-═NH3H2O | ||||
D、用惰性电极电解硫酸铜溶液:2C2++2H2O
|
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
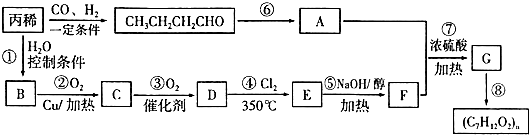
| 350℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 见图,接通电源,观察食盐水发生的变化.看见石墨棒一端产生黄绿色气体,然后用湿润的淀粉碘化钾试纸检验,试纸变蓝.通电前往U形管两端各滴入几滴酚酞试液,通电一段时间后,左侧U形管溶液颜色变红.
见图,接通电源,观察食盐水发生的变化.看见石墨棒一端产生黄绿色气体,然后用湿润的淀粉碘化钾试纸检验,试纸变蓝.通电前往U形管两端各滴入几滴酚酞试液,通电一段时间后,左侧U形管溶液颜色变红.查看答案和解析>>
科目:高中化学 来源: 题型:
 3名同学在用氯酸钾和二氧化锰混合加热制取氧气的过程中,发现生成的气体有刺激性气味,针对这一“异常现象”进行了实验探究及分析.
3名同学在用氯酸钾和二氧化锰混合加热制取氧气的过程中,发现生成的气体有刺激性气味,针对这一“异常现象”进行了实验探究及分析.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1,3-丁二烯和2-丁炔相互转化的焓变△H |
| B、1,3-丁二烯和2-丁炔分子的稳定性 |
| C、1,3-丁二烯和2-丁炔的燃烧热热值的相对大小 |
| D、2-丁炔中一个碳碳三键能与1,3-丁二烯中两个碳碳双键键能之和的相对大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电子不停地做高速运动 |
| B、电子在核外是分层排布的 |
| C、每个电子层作为最外层时,最多可容纳8个电子 |
| D、离原子核近的电子能量低,离原子核远的电子能量高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com