
 已知氧化性强弱顺序为BrO3->ClO3->Cl2>IO3->Br2>I2.某同学为验证其中某些离子的氧化性进行如下实验.向盛有30mL 0.2mol?L-1 KI溶液的锥形瓶中滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液至过量.
已知氧化性强弱顺序为BrO3->ClO3->Cl2>IO3->Br2>I2.某同学为验证其中某些离子的氧化性进行如下实验.向盛有30mL 0.2mol?L-1 KI溶液的锥形瓶中滴入几滴淀粉溶液和足量稀硫酸,再用滴定管逐滴加入KBrO3溶液至过量.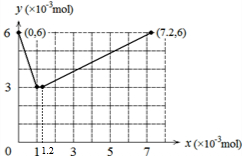
 .
.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
| A、CO2+H2O═H2CO3 化合反应 | ||||
B、Cu(OH)2
| ||||
C、Fe2O3+3CO
| ||||
| D、NaCl+AgNO3═AgCl↓NaNO3 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 4 |
| O | 2- 4 |
| A、3:2 | B、3:4 |
| C、1:2 | D、1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
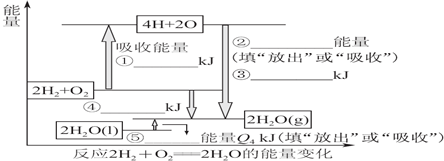
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一.
化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一.查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 | 结论 | |
| ① | 取少量上述漂白粉于试管中,加入适量1mol/L盐酸溶解后,再将产生的气体导入到澄清石灰水中 | 石灰水变浑浊 | |
| ② | 向上述反应后的试管滴入1~2滴品红溶液,振荡 | 品红褪色 | |
| 实验内容 | 将氯气持续通入淀粉碘化钾溶液 |
| 实验现象 | 溶液先变蓝,后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如右图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如右图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、反应③最多能产生0.05mol O2 |
| B、反应①的离子方程式为:Na+2H2O═Na++2OH-+H2↑ |
| C、Na2O2中阴阳离子数目之比为1:1 |
| D、①、②、③充分反应后所得溶液的质量分数从大到小:①>②>③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com