
 A、B、C、D、E五种常见元素的核电荷数依次增大.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子.请回答下列问题:
A、B、C、D、E五种常见元素的核电荷数依次增大.A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物,E的基态3d轨道上有2个电子.请回答下列问题:分析 A、B、C、D、E五种常见元素,它们的核电荷数依次增大.其中元素E的基态3d轨道上有2个电子,原子核外电子排布式为1s22s22p63s23p63d24s2,则E为Ti;B是地壳中含量最多的元素,则B为O元素;C是短周期中最活泼的金属元素,则C为Na;D与C可形成CD型离子化合物,则D为Cl;A的基态原子中有2个未成对电子,原子序数小于氧,原子核外电子排布式为1s22s22p2,故A为碳元素,据此解答.
解答 解:A、B、C、D、E五种常见元素,它们的核电荷数依次增大.其中元素E的基态3d轨道上有2个电子,原子核外电子排布式为1s22s22p63s23p63d24s2,则E为Ti;B是地壳中含量最多的元素,则B为O元素;C是短周期中最活泼的金属元素,则C为Na;D与C可形成CD型离子化合物,则D为Cl;A的基态原子中有2个未成对电子,原子序数小于氧,原子核外电子排布式为1s22s22p2,故A为碳元素.
(1)E的基态3d轨道上有2个电子,原子核外电子排布式为1s22s22p63s23p63d24s2,基态原子价层电子排布式为3d24s2,故答案为:3d24s2;
(2)CO2分子结构式为O=C=O,碳原子成2个δ键、没有孤对电子,故C原子采取sp杂化;
同周期随原子序数增大,第一电离能呈增大趋势,但N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能N>O>C,
故答案为:sp;N>O>C;
(3)H2O分子之间存在氢键,沸点高于HCl的,故答案为:H2O;H2O分子之间存在氢键;
(4)CO2形成的晶体属于分子晶体,NaCl属于离子晶体,通常情况下,离子晶体熔点大于分子晶体熔点,故CO2形成的晶体的熔点低于NaCl,故答案为:低于;CO2形成的晶体属于分子晶体,NaCl属于离子晶体;
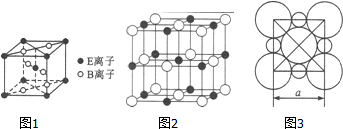
(5)该晶胞中Ti原子个数=1+8×$\frac{1}{8}$=2、O原子个数=2+4×$\frac{1}{2}$=4,则Ti、O原子个数之比=2:4=1:2,则化学式为TiO2,
TiCl4是制取航天航空工业材料的重要原料.取上述橙红色晶体,放在电炉中,通入Cl2和碳的单质后高温加热,可制得TiCl4,同时产生一种造成温室效应的气体,该气体为二氧化碳,该反应的化学方程式为:TiO2+C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+CO2,
故答案为:TiO2;TiO2+C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+CO2;
(6)由晶胞结构可知,Na+为黑球,Cl-为白球,晶胞中Na+离子数目=1+12×$\frac{1}{4}$=4,Cl-离子数目=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故晶胞质量=4×$\frac{58.5}{{N}_{A}}$g,则该晶体的密度=4×$\frac{58.5}{{N}_{A}}$g÷(acm)3=$\frac{234}{{N}_{A}×{a}^{3}}$g•cm-3,
故答案为:$\frac{234}{{N}_{A}×{a}^{3}}$.
点评 本题是对物质结构的考查,涉及晶胞计算、杂化轨道、电离能、核外电子排布、晶体性质等,推断元素是解题关键,注意利用均摊法进行晶胞计算.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
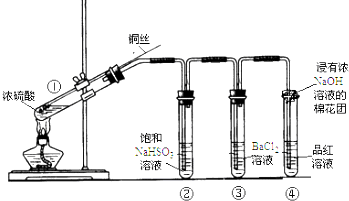
| 加入试剂 | 现象 | 反应的离子方程式 | |
| 第一份 | 加入NaOH溶液 | 有白色沉淀生成 | SO2+2OH-═SO32-+H2OBa2++SO32-═BaSO3↓ |
| 第二份 | 加入氯水 | 有白色沉淀生成 | SO2+Cl2+H2O═4H++2Cl-+SO42-Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口倒出 | |
| B. | 使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干 | |
| C. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| D. | 用10mL量筒量取9.2mL NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
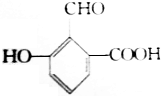 具有的三种官能团分别是:羟基、醛基和羧基,所以这种化合物可看作酚类、醛类和羧酸类.
具有的三种官能团分别是:羟基、醛基和羧基,所以这种化合物可看作酚类、醛类和羧酸类.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气 | |
| B. | 碳酸钠可作为治疗胃酸过多的药物,食品发酵剂 | |
| C. | 通过丁达尔效应可以鉴别稀豆浆和氢氧化铁胶体 | |
| D. | 焰色反应一定伴随着化学变化和物理过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+. Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用湿润的有色布条 | B. | 用湿润的蓝色石蕊试纸 | ||
| C. | 将气体通入硝酸银溶液 | D. | 用湿润的淀粉碘化钾试纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
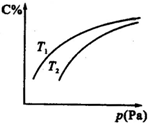
| A. | B一定为气体 | |
| B. | A一定为气体 | |
| C. | 若正反应方向△H<0,则T1>T2 | |
| D. | 压强增大时,混合气体的平均相对分子质量减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com