
| A、同压强、同体积的N2O和CO2 |
| B、同温度、同体积的氮气和氯气 |
| C、同体积、同密度的乙烯和丙烯 |
| D、同温度、同压强、同体积的氦气和氢气 |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、用精密pH试纸测得某盐溶液的pH=9.26 |
| B、用酸式滴定管量取20.00mLNa2CO3溶液 |
| C、甲基橙作指示剂,用标准NaOH溶液(碱式滴定管中)滴定未知浓度的醋酸(锥形瓶中),终点时的颜色变化为:橙色→黄色 |
| D、中和滴定实验时,锥形瓶用蒸馏水洗涤2-3次后,就可以直接加入一定体积的标准液或待测液了,不需要对锥形瓶进行润洗,也不需要干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:
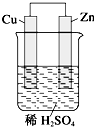 如图是Zn和Cu形成的原电池,则下列结论中正确的是( )
如图是Zn和Cu形成的原电池,则下列结论中正确的是( )| A、①②③ | B、②④ |
| C、④⑤⑥ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应能在瞬间完成,并产生大量气体 |
| B、生成标准状况下2.24L气体,该反应转移电子的物质的量为0.5mol |
| C、该反应中的氧化剂为KNO3 |
| D、被氧化和被还原的N原子的物质的量之比为15:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三种元素按原子个数比1:1:1所形成的化合物水溶液显碱性 |
| B、X、Z形成的化合物一定只含离子键 |
| C、同周期元素中Y的最高价含氧酸的酸性最强 |
| D、Y单质有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与稀盐酸反应:Fe3O4+8H+═Fe3++4H2O | 正确 |
| B | 向碳酸镁中加入稀盐酸:CO32-+2H+═CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
| C | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2++SO42-═BaSO4↓ | 正确 |
| D | 澄清石灰水与少量的CO2反应Ca(OH)2+CO2=CaCO3↓+H2O | 错误,少量的CO2生成物应为Ca(HCO3)2 |
| A、A | B、B | C、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Al3+、Cl?、SO32- |
| B、Na+、K+、OH?、[Al(OH)4]- |
| C、H+、K+、SO42-、NO3? |
| D、Na+、NH4+、Cl-、OH? |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com