
| A. | 盐酸的物质的量浓度是0.5mol•L-1 | B. | 氢氧化钠溶液的体积是250mL | ||
| C. | 铁和硅的物质的量之比为2:1 | D. | 铁和硅的质量之比为1:2 |
分析 根据发生的反应2Al+6HCl═2AlCl3+3H2↑、Fe+2HCl═FeCl2+H2↑、Si+2NaOH+H2O═Na2SiO3+2H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,酸、碱恰好完全反应,则在与酸的反应中Fe和Al,Al和Si完全反应,再利用放出氢气的量来计算.
解答 解:发生反应为:2Al+6HCl═2AlCl3+3H2↑、Fe+2HCl═FeCl2+H2↑、Si+2NaOH+H2O═Na2SiO3+2H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑,
A.标准状况下1.12L氢气的物质的量为:$\frac{1.12L}{22.4L/mol}$=0.05mol,根据H元素守恒可知参加反应的HCl的物质的量为0.1mol,浓度为:$\frac{0.1mol}{0.1L}$=1mol/L,故A错误
B.根据反应Si+2NaOH+H2O═Na2SiO3+2H2↑、2Al+2NaOH+2H2O═2NaAlO2+3H2↑可知,无法根据生成氢气的量计算消耗的NaOH的物质的量,故B错误;
C.由于等质量的样品分别投入稀盐酸和氢氧化钠溶液中,恰好完全反应且反应后都放出标准状况下1.12LH2,则反应Fe+2HCl═FeCl2+H2↑、Si+2NaOH+H2O═Na2SiO3+2H2↑中生成的氢气相同,若都生成nH2,n(Fe)=n mol,n(Si)=0.5nmol,则粗铝中铁和硅的物质的量比为2mol:1mol=2:1,故C正确;
D.根据C的计算可知,铁和硅的物质的量之比为2:1,D错误;
故选C.
点评 本题考查Al、Fe、Si的化学性质、化学方程式的计算,题目难度中等,明确发生的化学反应及信息中生成氢气的量相同是解答本题的关键,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:解答题
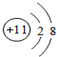 ,写出Cl在周期表中的位置第三周期VIIA族.
,写出Cl在周期表中的位置第三周期VIIA族.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
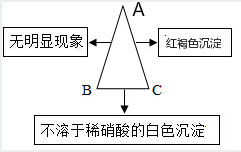 现有A、B、C三种物质,已知A是一种氯化物,B是一种钠盐,C是一种碱,下图表示的是A、B、C的溶液两两混合的实验现象.请回答下列个小题:
现有A、B、C三种物质,已知A是一种氯化物,B是一种钠盐,C是一种碱,下图表示的是A、B、C的溶液两两混合的实验现象.请回答下列个小题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸与碱恰好中和时所放出的热量叫中和热 | |
| B. | 化学反应中能量变化的大小与反应物的质量无关 | |
| C. | 伴有能量变化的过程都是化学变化 | |
| D. | 化学反应中的能量变化,主要是由化学键变化引起的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C0(NH2)2 | B. | NH4NO3 | C. | NH4HCO3 | D. | (NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
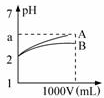 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )| A. | a=5时,A是强酸,B是弱酸 | |
| B. | 若A、B都是强酸,则5>a>2 | |
| C. | 稀释后,A酸溶液的酸性比B酸溶液强 | |
| D. | A、B两种酸溶液的物质的量浓度一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com