



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
| A��-218 kJ/mol |
| B��-109 kJ/mol |
| C��+218 kJ/mol |
| D��+109 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڼ�����Һ�У�HCO3-��K+��C1-��Na+ |
| B�������۷�Ӧ�ų���������ɫ��Һ�У�NO3-��K+��Na+��SO42- |
| C����c��H+��/c��OH-���T1��1013����Һ�У�NH4+��Br-��C1-��K+ |
| D��ͨ��SO2����Һ�У�Ca2+��C1-��NO3-��A13+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����ȼ��н�100mL 0.50mol?L-1��CH3COOH��Һ��100mL 0.55mol?L-1��NaOH��Һ��ϣ��¶ȴ�298.0K������300.7K����֪���ȼƵ����ݳ��������ȼƸ�����ÿ����1K����Ҫ����������150.5J?K-1����Һ�ܶȾ�Ϊ1g?mL-1��������Һ�ı�����c=4.184J?��g?K��-1��
�����ȼ��н�100mL 0.50mol?L-1��CH3COOH��Һ��100mL 0.55mol?L-1��NaOH��Һ��ϣ��¶ȴ�298.0K������300.7K����֪���ȼƵ����ݳ��������ȼƸ�����ÿ����1K����Ҫ����������150.5J?K-1����Һ�ܶȾ�Ϊ1g?mL-1��������Һ�ı�����c=4.184J?��g?K��-1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
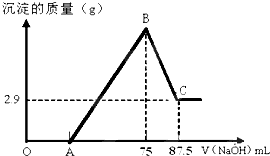 ��һ����þ�����Ļ�Ϸ�ĩ����50mLδ֪Ũ�ȵ������У����裬�õ�������Һ���ڴ���Һ����ε���8mol/L��NaOH��Һ���μ�NaOH��Һ����������������������ͼ��ʾ����ش��������⣺
��һ����þ�����Ļ�Ϸ�ĩ����50mLδ֪Ũ�ȵ������У����裬�õ�������Һ���ڴ���Һ����ε���8mol/L��NaOH��Һ���μ�NaOH��Һ����������������������ͼ��ʾ����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
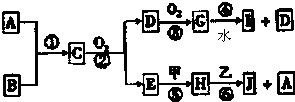
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Cl2+H2O�THCl+HClO |
| B��2Na+2H2O�T2NaOH+H2�� |
| C��P2O5+3H2O�T2H3PO4 |
| D��3NO2+H2O�T2HNO3+NO |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com