
 ̽��ʵ��չʾ�˻�ѧ������������������ʵ��Ĺ�����Ҳ����������̽��������
̽��ʵ��չʾ�˻�ѧ������������������ʵ��Ĺ�����Ҳ����������̽��������| ʵ����� | ��ˮ | ��ˮ |
| ��ʼ | ��ɫ��ɢ���� | ��ɫ��ɢ�Ͽ� |
| ���÷��� | ���վ���Ϊ��ɫ�����ȡ�����Һ�� | |
���� ѡ�õ�����ҩƷŨ�����Ũ��ˮ�����лӷ��ԣ��ֱ��ܻӷ����Ȼ�������Ͱ��������߽Ӵ��ᷴӦ����һ�ְ�ɫ�Ĺ����Ȼ�泥�ͨ��C���������̽϶�����жϰ��������˶��ÿ�һЩ�����ݰ�������Է����������Ȼ������Է���������С���ɵõ����ӵ��˶���������Է��������Ĺ�ϵ����չ̽���У���������Ʒ��ֱ���뵽��������ˮ����ˮ�У���������ˮ��Ʒ����ɢ�Ͽ죬˵���¶ȸ߷����˶����ʸ��죮
��� �⣺��1����������Է�������ΪMr��NH3��=Ar��N����1+Ar��H����3=��14��1��+��1��3��=17���Ȼ������Է�������ΪMr��HCl��=Ar��H����1+Ar��Cl����1=��1��1��+��35.5��1��=36.5���ʰ�������Է�������С���Ȼ������Է�������������C�����ְ��̽϶࣬��մ�а�ˮ������Զ��˵�����������˶���Ҫ�죬�õ����ۣ���Է�������ԽС���˶��ٶ�Խ�죬
�ʴ�Ϊ��С�ڣ�С���죻
��2���������Ȼ��ⷴӦ�����Ȼ�泥���Ӧ�Ļ�ѧ����ʽΪ��NH3+HCl�TNH4Cl��
�ʴ�Ϊ��NH3+HCl�TNH4Cl��
��չ̽������������Ʒ��ֱ���뵽��������ˮ����ˮ�У��۲쵽Ʒ������ˮ��Ҫ������ˮ����ɢ�ÿ�һЩ��������ˮ���¶ȱ���ˮ��Ҫ�ߣ��ݴ˿�֪���¶�Խ�ߣ�Ʒ������˶���Խ�죬
�ʴ�Ϊ���¶�Խ�ߣ����ӵ��˶�Խ�죮
���� ���⿼��ѧ����ʵ��̽����ͨ��ʵ����������ݵķ������õ���صĽ��۵�������Ҫ�����Ҫ������Ŀ�е���֪�����⣬��Ҫ����һЩ���ص����ݣ��籾�����������ʵ���Է������������⣬��չ̽���еĿ��Ʊ������ȽϷ�������һ�ֳ��õ�ʵ�鷽����


 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���̴��ŷ� | B�� | �ð�ˮ���պ��ŷ� | ||
| C�� | ���ռ����պ��ŷ� | D�� | �û���̿���պ��ŷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ի�ɫ����Һ��Na+��CO32-��NO3-��SO32- | |
| B�� | ����ˮ�������c��H+��=1��10-12mol/L����Һ��Fe3+��ClO-��Na+��SO42- | |
| C�� | �������������H2����Һ�У�Na+��K+��SO42-��Cl- | |
| D�� | ������ˮ�У�Cl-��Na+��NO3-��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ����ȼ�ϵ��ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش�
ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã���ͼΪ����ȼ�ϵ��ʾ��ͼ���õ�ص缫�����һ��ϸС�IJ��ۣ����������������ǿ�������ȶ�����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��NO3-��Al3+��K+ | B�� | Na+��ClO3-��ClO-��ClO4- | ||
| C�� | K+��Cr2O72-��I-��Na+ | D�� | Na+��SO32-��SO42-��NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
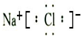 ��2��H2H��H��3��MgCl2
��2��H2H��H��3��MgCl2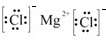
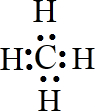 ��5��CO2
��5��CO2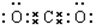 ��6��Na2O
��6��Na2O
 ��O=C=O��
��O=C=O���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com