
【题目】在20 L的密闭容器中按物质的量之比1∶2充入CO和H2,发生反应CO(g)+2H2(g)CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如下表所示。下列说法正确的是( )
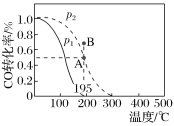
p2和195 ℃时n(H2)
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 5 | 4 | 4 |
A.p2和195 ℃时,0~3 min,反应速率v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
B.p1<p2,ΔH>0
C.195 ℃、p2时,在B点:v正>v逆
D.在p2和195 ℃时,该反应的平衡常数为25
【答案】D
【解析】
A.0~3min,Δn(H2)=4mol,Δc(H2)=![]() =0.2 mol·L-1,v(H2)=
=0.2 mol·L-1,v(H2)=![]() ,v(H2) :v(CH3OH)=2:1,则v(CH3OH)≈0.033 mol·L-1·min-1,故A错误;
,v(H2) :v(CH3OH)=2:1,则v(CH3OH)≈0.033 mol·L-1·min-1,故A错误;
B.由任意一条曲线知,随温度升高,CO转化率减小,故ΔH<0,由于增大压强时,平衡右移,故p1<p2,故B错误;
C.从B点到A点,CO转化率减小,反应向左进行,故v正<v逆,故C错误;
D.达到平衡时,CO、H2、CH3OH的平衡浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.1 mol·L-1,则平衡常数K=![]() =
=![]() =
=![]() =25,故D正确;
=25,故D正确;
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氨气是极易溶于水的气体,常温常压下,1体积水大约能溶解700体积的氨气。
(1)实验室可在浓氨水中加入固体NaOH快速制取氨气,请用化学平衡移动原理简述原因___。
(2)甲、乙两瓶氨水的浓度分别为1mol·L-1和0.1mol·L-1,则甲、乙两瓶氨水中c(OH-)之比___(填“>”、“<”或“=”)10。
(3)向10mL0.1mol/L的氨水中逐滴加入20mL0.1mol/L的醋酸,溶液导电性的变化是___。写出二者反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某锂离子电池正极材料有钴酸锂(LiCoO2)、石墨和铝箔等,该电池充电时负极(阴极)反应为6C+xLi++xe- = LixC6,锂电池充放电过程中发生LiCoO2与Li1-xCoO2之间的转化。现利用以下工艺回收正极材料中的某些金属资源。
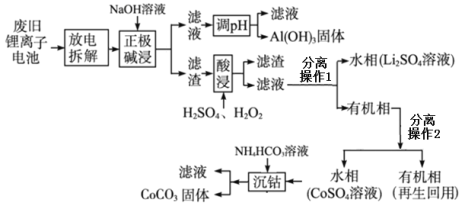
回答下列问题:
(1)放电时电池总反应方程式_______________;该工艺首先将废旧电池“放电处理”的目的除安全外还有_______________。
(2)写出“正极碱浸”过程中发生反应的离子方程式_______________。
(3) 分离操作1是_______________;“酸浸”步骤发生的氧化还原反应化学方程式是_______________。
(4)“酸浸”时若用盐酸代替H2SO4和H2O2的混合液,缺点是_______________。
(5)“沉钴”过程中的实验现象有_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C三种分子所含原子的数目依次为1、3、6,且分子中均含有18个电子,B、C是由两种元素组成的,且分子中两种元素原子的个数比均为1:2。请回答下列问题。
(1)A的分子式是__________,写出A原子的价电子排布式:__________
(2)B分子的中心原子的杂化类型是__________,分子的空间构型是__________,该分子属于__________(填“极性”或“非极性”)分子。
(3)C的化学式是__________,分子中含有的化学键类型是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据杂化轨道理论和价电子对互斥理论模型判断,下列分子或离子的中心原子杂化方式及空间构型正确的是( )
选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥理论模型 | 分子或离子的空间构型 |
A | H2O | sp1 | 直线形 | 直线形 |
B | BBr3 | sp2 | 平面三角形 | 三角锥形 |
C | PCl3 | sp2 | 四面体形 | 平面三角形 |
D | CO32- | sp2 | 平面三角形 | 平面三角形 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。
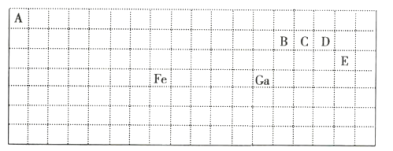
根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为__。
(2)Fe元素位于周期表的__区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为__。与CO分子互为等电子体的分子为__(填化学式)。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有__。
(4)ED4-的价电子对互斥理论模型为__。B、C、D、E中两种原子相互结合形成的分子中,所有原子都满足最外层8电子稳定结构的是__(写2种,填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是
A.  在NaCl晶体中,距Na+最近的Cl-形成正八面体
在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.  在CaF2晶体中,每个晶胞平均占有4个Ca2+
在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.  在金刚石晶体中,碳原子与碳碳键数目比为1∶2
在金刚石晶体中,碳原子与碳碳键数目比为1∶2
D.  由E原子和F原子构成的气态团簇分子的分子式为EF或FE
由E原子和F原子构成的气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用键线式表示,如:
结构简式 |
|
|
|
键线式 |
|
|
|
(1)![]() 的分子式为___________。
的分子式为___________。
(2)已知三个乙炔分子反应生成苯,试写出三个丙炔分子反应生成的芳香烃分子的键线式:__________(填一种即可)。
(3)由![]() 以及必要的无机试剂可合成
以及必要的无机试剂可合成 ,写出第一步合成反应的化学方程式:________。
,写出第一步合成反应的化学方程式:________。
(4)A为![]() 的一种同分异构体,A的一氯代物有三种,且A与
的一种同分异构体,A的一氯代物有三种,且A与![]() 按物质的量之比为
按物质的量之比为![]() 加成得到的产物只有一种(不考虑顺反、立体异构),则A可能的结构简式有_____________。
加成得到的产物只有一种(不考虑顺反、立体异构),则A可能的结构简式有_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.制药厂常用氯乙烷来制备喷雾剂,主要是由于氯乙烷合成简单、价格便宜
B.![]() 的同分异构体有3种
的同分异构体有3种
C.甲苯在光照下与![]() 发生的主要反应为苯环上引入氯原子的取代反应
发生的主要反应为苯环上引入氯原子的取代反应
D.有机物![]() 在
在![]() 的乙醇溶液中发生反应最多得到3种有机产物
的乙醇溶液中发生反应最多得到3种有机产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com