
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③碘的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏B.分液、蒸馏、萃取
C.萃取、蒸馏、分液D.蒸馏、萃取、分液
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用软锰矿[主要成分MnO2,还含Fe2O3、Cu2(OH)2CO3及少量不溶于水和酸的杂质]和酸洗厂废酸液(含1mol/LH2SO4的FeSO4溶液)联合生产硫酸锰和铁红(Fe2O3),生产过程如下图:
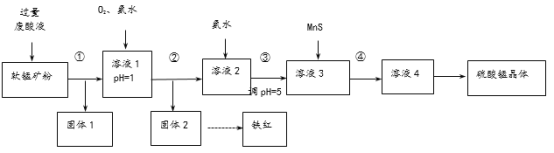
Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.3 | 6.3 | 4.7 | 2.7 |
完全沉淀时 | 9.8 | 8.3 | 6.7 | 3.6 |
(1)过程①~④所涉及的实验操作方法中,包含过滤的有______(写序号)。
(2)溶液1中,先通入O2,其作用是_______。
(3)由固体2得到铁红的化学方程式是_______。
(4)下列说法正确的是______(填字母)。
a.过程①中有氧化还原反应发生
b.加入MnS的目的是除去溶液中的Cu2+,增大Mn2+
c.溶液1中含有的阳离子主要是Fe2+、Fe3+、Cu2+、Mn2+、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解法精炼铜的下列说法正确的是( )
A. 粗铜作阳极,纯铜作阴极,硫酸铜为电解质溶液
B. 纯铜作阳极,粗铜作阴极,硫酸铜为电解质溶液
C. 电解结束后,溶液中Cu2+浓度不变
D. 电解结束后,溶液中Cu2+浓度变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)为白色晶体,是强氧化剂,常用作火箭发射的推进剂。已知:①NH4ClO4在400℃时开始分解,产物为N2、Cl2、O2、H2O;②Mg3N2易水解。请用下图所示装置设计实验证明分解产物中含有Cl2、H2O以及装置A中生成了Mg3N2(装置不重复使用)。
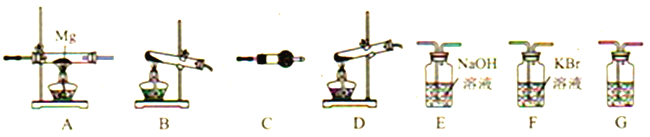
(1)写出高氯酸铵分解的化学方程式__________。
(2)高氯酸铵分解选择的装置是__________(填字母)。
(3)按气流从左到右,装置的连接顺序是:分解装置→_____→_____→_____→_____→_____。______________
(4)C中所放的试剂是__________,G的作用是__________ 。
(5)能证明有Cl2产生的现象是__________。
(6)要证明装置A中生成了Mg3N2需要进行的实验操作以及对应的实验现象是__________。
(7)某实验宣存放的高氯酸铵样品中含有少量杂质,已知可用蒸馏法测定NH4ClO4的含量,其测定流程如下(杂质不参加反应),则样品中NH4ClO4的含量(w)为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应:X+2Y2Z(△H<0),其中Z显气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图,下列判断正确的是( ) 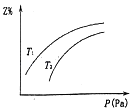
A.Y一定呈气态
B.T1大于T2
C.升高温度,该反应的化学平衡常数增大
D.当c(X):c(Y):c(Z)=1:2:2时,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0.20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)该反应的化学方程式为 , 表中bc(填“<”、“=”、“>”).
(2)20s时,N2O4的浓度为mol/L,0~20s内N2O4的平均反应速率为 .
(3)该反应的平衡常数表达式K= , 在80℃时该反应的平衡常数K值为(保留2位小数).
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时 .
A.N2O4的转化率越高
B.NO2的产量越大
C.N2O4与NO2的浓度之比越大
D.正反应进行的程度越大.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+ , 然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+).现用如图装置模拟上述过程,则: 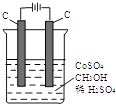
Co2+在阳极的电极反应式为:;除去甲醇的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列数据: Fe(s)+ ![]() O2(g)═FeO(s)△H=﹣272kJmol﹣1
O2(g)═FeO(s)△H=﹣272kJmol﹣1
2Al(s)+ ![]() O2(g)═Al2O3(s)△H=﹣1675kJmol﹣1
O2(g)═Al2O3(s)△H=﹣1675kJmol﹣1
则2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)的△H是( )
A.+859 kJmol﹣1
B.﹣859 kJmol﹣1
C.﹣1403 kJmol﹣1
D.﹣2491 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E5种微粒,它们可能是原子或离子,并且组成它们的元素的原子序数都小于18。A微粒的最外层电子数比次外层多5个;金属原子B的原子核内质子数比前一周期的同族元素多8个,其单质不能从CuSO4溶液中置换出Cu;C元素有3种同位素:C1、C2、C3,C1的质量数分别为C2、C3的![]() 和
和![]() ;D元素的气态氢化物溶于水后显碱性;E是由两种不同元素组成的带负电荷的微粒,它共有2个原子核10个电子,E极易与C+结合成中性微粒。
;D元素的气态氢化物溶于水后显碱性;E是由两种不同元素组成的带负电荷的微粒,它共有2个原子核10个电子,E极易与C+结合成中性微粒。
(1)写出五种微粒的表示符号:A________、B________、C________、D________、E________。
(2)写出C的同位素名称:C1________、C2________、C3________。
(3)C和D形成的10个电子的分子的化学式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com