
| A. | 放出碱液的滴定管开始有气泡,发出液体后气泡消失 | |
| B. | 滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定 | |
| C. | 锥形瓶用蒸馏水洗涤后,直接加入待测溶液滴定 | |
| D. | 滴定管用蒸馏水洗涤后,直接注入待测液,取20.00 mL进行滴定 |
分析 根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差,据此解答.
解答 解:A.放出碱液的滴定管开始有气泡,发出液体后气泡消失,导致量取的待测液体积偏小,消耗的标准液体积偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知溶液浓度偏低,故A不选;
B.滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定,都在标准液浓度降低,消耗的标准液体积偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知溶液浓度偏高,故B选;
C.锥形瓶用蒸馏水洗涤后,直接加入待测溶液滴定,对消耗的标准液体积不产生影响,溶液浓度不变,故C不选;
D.滴定管用蒸馏水洗涤后,直接注入待测液,取20.00 mL进行滴定,导致待测液被稀释,浓度降低,实际消耗的标准液体积偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$可知溶液浓度偏低,故D不选;
故选:B.
点评 本题考查了中和滴定实验误差分析,准确判断错误操作导致消耗标准液体积的影响是解题关键,题目难度中等.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
 已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )
已知如表25℃时某些弱酸的电离平衡常数.如图表示常温时,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.依据所给信息,下列说法正确的是( )| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
| A. | 如图中的两种酸分别和等浓度的NaOH溶液刚好完全反应,消耗碱的体积相等 | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | a、b、c三点所示溶液中水的电离程度c>a>b | |
| D. | 图象中,Ⅰ表示CH3COOH,Ⅱ表示HClO,且溶液导电性:c>b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Na2S2O3起始读数 | Na2S2O3 终点读数 | |
| 第一次 | 0.10mL | 18.30mL |
| 第二次 | 0.30mL | 18.30mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

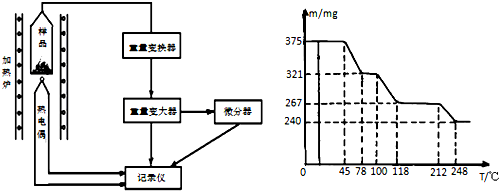
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
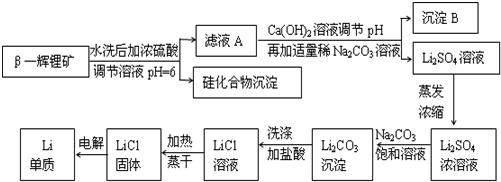
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
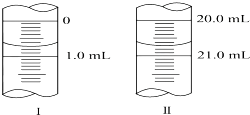 在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:
在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度.在H2SO4溶液中,反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
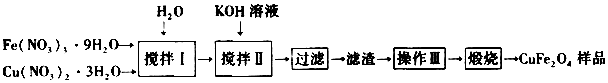
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com