
【题目】已知NA为阿伏加德罗常数的数值,下列说法正确的是
A. 56g铁在足量氧气中燃烧,转移的电子数为2NA
B. lg氢气含有NA个氢气分子
C. 标准状况下,22.4L水含有1mol水分子
D. 2mol钠与过量稀盐酸反应生成NA个氢气分子
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】过氧化氢是一种绿色氧化剂、还原剂,工业上有多种方法制备H2O2。
(1)①研究表明,H2O2相当于二元弱酸,则它的一级电离方程式为_______________,已知常温下1 L的H2O2相当于48.3 mol,其K1≈1.67×10-12。则该温度下H2O2中c(H+)约为__________,写出它与足量Ba(OH)2反应的化学方程式:_____________。
②乙基蒽醌法是制备过氧化氢最常用的方法,其主要过程可以用下图表示,写出此过程的总化学方程式:___________________________________________。

③空气阴极法制备H2O2是一种环境友好型、节能型制备方法,电解总方程式为3H2O+3O2![]() 3H2O2+O3,则阳极上电极反应式为________________________。
3H2O2+O3,则阳极上电极反应式为________________________。
(2)氧也能与钾元素形成K2O、K2O2、KO2、KO3等氧化物,其中KO2是一种比Na2O2效率高的供氧剂,写出它与CO2反应的化学方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中下列物质的有关说法错误的是
A. 食盐和白醋都可作调味剂
B. 糖类和蛋白质都可发生水解
C. 液化石油气和天然气都是含烃混合物
D. 双氧水和碘酒都可作医用消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO和KClO3,且![]() 的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
的值与温度高低有关.当n(KOH)=amol时,下列有关说法错误的是( )
A. 若某温度下,反应后 =2,则溶液中
=2,则溶液中 =0.2
=0.2
B. 参加反应的氯气的物质的量等于0.5a mol
C. 改变温度,反应中转移电子的物质的量ne的范围: ![]() a mol≤ ne ≤
a mol≤ ne ≤![]() a mol
a mol
D. 改变温度,产物中KClO3的最大理论产量为![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。请回答下列问题:
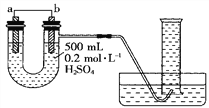
(1)b电极材料为__________,其电极反应式为_________________________。
(2)当量筒中收集到672 mL(标准状况下)气体时,通过导线的电子的物质的量为__________,此时a电极质量减少__________g。
II.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有:_____________________________________________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是_________________________________________;
(3)要加快上述实验中气体产生的速率,还可采取的措施有_____________________(答两种);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是
A.分子中碳原子不在一条直线上B.比丁烷更易液化
C.1mol丙烷完全燃烧需消耗氧气5molD.光照下能够发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钠与水的反应是中学化学中的一个重要反应。高一化学教材中该实验曾出现过几种不同的演示方法。分别如下图中(A)(B)(C)所示:
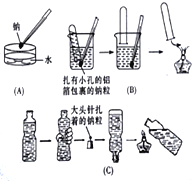
(1)现按图(A)所示的方法,在室温时,向盛有饱和Na2CO3溶液(滴有几滴酚酞)的烧杯中,加入一小块金属钠。
①下列现象描述正确的是_______(填字母代号)。
A.钠浮在液面上,并四处游动,最后消失 B.反应过程中钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色 D.恢复到室温时,烧杯底部有固体物质析出
②请补充并完成该实验从试剂瓶中取出钠到向烧杯中投入钠的有关操作:
用镊子从试剂瓶中取出一小块钠→_______________→用镊子夹取切好的金属钠投入到盛有饱和Na2CO3溶液的烧杯中。
(2)按图(C)所示的方法进行该实验,若500mL的矿泉水瓶开始时装有477.6mL水,要使倒置的矿泉水瓶正好恢复原状,假设矿泉水瓶内外均为标准状况,则大头针上扎着的钠粒质量为_______g。
(3)1998年全国高考试题中的实验题就是根据图(B)的原理设计的。题目及部分答案如下:
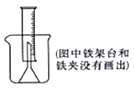
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数。现有下列实验用品:中学化学实验常用仪器、800毫升烧杯、100毫升量筒、短颈玻璃漏斗、长颈漏斗、玻璃棒、铜网、铝锌合金样品、浓盐酸(密度1.19克/毫升)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100毫升)
Ⅰ.补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在800毫升烧杯底部,把短颈漏斗倒扣在样品上面。……
[答案]
Ⅰ.②往烧杯中注入水,直至水面没过漏斗颈。[评分标准,凡加水改为加酸者,不论其他后续步骤是否正确,本小题一律0分]
③在100毫升量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中。烧杯中水面到杯口至少保留约100毫升空间。
④将“仅器A”插入烧杯并接近烧杯底部,通过它慢慢加入浓盐酸,至有气体产生。
回答下列问题:
a.为什么在“②往烧杯中注入水,直至水面没过调斗颈”这一步中改加水为加酸会得0分:______________________________________________________________________________。
b.“仪器A”可以是________________________。
c.合金样品用铜网包裹的目的是____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com