
热化学方程式C(s)+H2O(g) CO(g)+H2(g) ΔH="+131.3" kJ·mol-1表示的
CO(g)+H2(g) ΔH="+131.3" kJ·mol-1表示的
为( )
| A.碳与水反应吸收131.3 kJ的热量 |
| B.1 mol碳和1 mol水反应吸收131.3 kJ的热量 |
| C.1 mol固态碳与1 mol水蒸气反应产生一氧化碳气体和氢气,吸收131.3 kJ的热量 |
| D.固态碳和气态水各1 mol反应,放出131.3 kJ的热量 |
科目:高中化学 来源: 题型:单选题
盖斯定律认为:不管化学过程是一步或分为数步完成,这个过程的热效应是相同的。
已知:H2O(g)= H2O(l) △H1 =-Q1 kJ·mol-1(Q1>0)
C2H5OH(g)= C2H5OH(l) △H2 =-Q2 kJ·mol-1(Q2>0)
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3 = -Q3 kJ·mol-1(Q3>0)若使23g液态乙醇完全燃烧,最后恢复到室温,则放出的热量为(kJ)
| A.Q1+ Q2+Q3 | B.0.5(Q1+Q2+Q3 ) |
| C.0.5 Q1-1.5 Q2+0.5Q3 | D.1.5 Q1-0.5 Q2+0.5Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知下列热化学方程式:
①C(s)+O2(g)==CO2(g)△H= —393.5kJ/mol
②CO(g)+ 1/2 O2(g)="=" CO2(g)△H= —283.0kJ/mol
③2Fe(s)+3CO(g)==Fe2O3(s)+3C(s)△H= —489.0kJ/mol
则4Fe(s)+3O2(g)==2Fe2O3(s)的反应热ΔH为( )
| A.-1641.0kJ/mol | B.+3081kJ/mol |
| C.+663.5kJ/mol | D.-2507.0kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l) ΔH1
2H2(g)+O2(g)=2H2O(g) ΔH2
C(s)+O2(g)=CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为( )。
| A.12ΔH3+5ΔH2-2ΔH1 | B.2ΔH1-5ΔH2-12ΔH3 |
| C.12ΔH3-5ΔH2-2ΔH1 | D.ΔH1-5ΔH2-12ΔH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )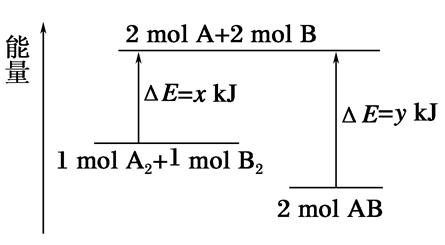
| A.该反应是吸热反应 |
| B.断裂1mol A—A键和1mol B—B键能放出xkJ的能量 |
| C.断裂2mol A—B键需要吸收ykJ的能量 |
| D.2mol AB的总能量高于1 mol A2和1mol B2的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据碘与氢气反应的热化学方程式
(ⅰ)I2(g)+H2(g)  2HI(g) ΔH=-9.48 kJ·mol-1
2HI(g) ΔH=-9.48 kJ·mol-1
(ⅱ)I2(s)+H2(g)  2HI(g) ΔH=+26.48 kJ·mol-1
2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是( )
| A.1 mol I2(s)中通入2 g H2(g),反应吸热26.48 kJ |
| B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
| C.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 |
| D.反应(ⅰ)放出的热量多,所以产物的能量低,比反应(ⅱ)的产物更稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某一化学反应在不同条件下的能量变化曲线如下图所示。下列说法正确的是( )
| A.化学催化比酶催化的效果好 |
| B.使用不同催化剂可以改变反应的热效应 |
| C.使用不同催化剂可以改变反应的能耗 |
| D.反应物的总能量低于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知甲烷燃烧生成二氧化碳和液态水放出的热量为55.625 kJ·g-1。下列热化学方程式中不正确的是( )
A.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH ="-890" kJ/mol CO2(g)+2H2O(l) ΔH ="-890" kJ/mol |
B.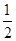 CH4(g)+O2(g) CH4(g)+O2(g) 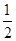 CO2(g)+H2O(l) ΔH="-445" kJ/mol CO2(g)+H2O(l) ΔH="-445" kJ/mol |
C.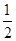 CO2(g)+H2O(l) CO2(g)+H2O(l) 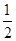 CH4(g)+O2(g) ΔH="+445" kJ/mol CH4(g)+O2(g) ΔH="+445" kJ/mol |
D.CH4(g)+2O2(g) CO2(g)+2H2O(l) ΔH="-55.625" kJ/mol CO2(g)+2H2O(l) ΔH="-55.625" kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)
ΔH=-57.3 kJ/mol下列结论正确的是( )
| A.碳的燃烧热的数值大于110.5 kJ/mol |
| B.①的反应热ΔH为221 kJ/mol |
| C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com