
| A�� | NaB��Һ��pH=8��c��Na+��-c��B-��=9.9��10-6mol•L-1 | |
| B�� | pH��ȵĢ�NH4C1���ڣ�NH4��2SO4����NH4HSO4������Һ�У�c��NH4+����С˳��Ϊ����=�ڣ��� | |
| C�� | Na2CO3��Һ�У�2c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | 10mLpH=12������������Һ�м���pH=2��HA��pH�պõ���7��������Һ���V���ܣ���20mL |
���� A��NaB��Һ��PH=8��B-����ˮ����Һ�Լ��ԣ�������Һ�е���غ���������
B���������Ƕȿ��ǣ�һ����ͬpH�ģ�NH4��2SO4��NH4Cl��Һ��ˮ��̶��Ƿ���ȣ�����NH4HSO4����ʱ����H+ʹ��Һ�����ԣ�NH4+��ˮ�ⱻ���ƣ��Դ������
C��Na2CO3��Һ�д��������غ�n��Na��=2n��C����̼Ԫ�����д�����ʽ�ܺ͵���̼Ԫ��������
D�����HA��ǿ�ᣬ����Һ��pH=7��HA���Ϊ10mL�����HA�����ᣬ����Һ��pH=7ʱ��HA���С��10mL��
��� �⣺A��NaB��Һ��PH=8��B-����ˮ����Һ�Լ��ԣ���Һ�д��ڵ���غ㣬c��Na+��+c��H+��=c��OH-��+c��B-����c��Na+��-c��B-��=c��OH-��-c��H+��=10-6mol/L-10-8mol/L=9.9��10-7mol•L-1����A����
B����ͬpH�ģ�NH4��2SO4��NH4Cl��Һ�У�����ǿ�������Σ�������Һ�ʵ����Կ��ж϶���NH4+Ũ����ȣ�����NH4HSO4����ʱ����H+ʹ��Һ�����ԣ�NH4+��ˮ�ⱻ���ƣ����NH4HSO4��NH4+��Ũ��С�ڣ�NH4��2SO4����=�ڣ��ۣ���B��ȷ��
C��Na2CO3��Һ�д��������غ㣬c��Na+��=2c��CO32-��+2c��HCO3-��+2c��H2CO3������C����
D�����HA��ǿ�ᣬ����Һ��pH=7��HA���Ϊ10mL�����HA�����ᣬ����Һ��pH=7ʱ��HA���С��10mL������������Һ�������V��20ml����D����
��ѡB��
���� ���⿼��������Ũ�ȴ�С�Ƚϣ���Ŀ�Ѷ��еȣ���ȷ����غ㡢�����غ㼰�ε�ˮ��ԭ��Ϊ���ؼ���DΪ�״��㣬ע��HA������ǿ��������������ѧ���ķ������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��������Ũ��Ϊ0.1mol/L�����ΪVL�İ�ˮ����������μ���һ��Ũ�ȵ����ᣬ�õ���ͼ�ĵζ����ߣ�����d��ʱ������Һǡ����ȫ��Ӧ������ͼ��ش��������⣺
��������Ũ��Ϊ0.1mol/L�����ΪVL�İ�ˮ����������μ���һ��Ũ�ȵ����ᣬ�õ���ͼ�ĵζ����ߣ�����d��ʱ������Һǡ����ȫ��Ӧ������ͼ��ش��������⣺| ����Ũ�ȴ�С˳�� | ���ʻ�ѧʽ | ��Һ��pH |
| c ��NH4+����c ��OH-����c ��CI-����c ��H+�� | �� | ��7 |
| �� | �� | =7 |
| �� | NH4Cl | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ����ͼ��ʾ��
һ���¶��£�ij�ݻ�Ϊ2L���ܱ������ڣ�ijһ��Ӧ��M��N�����ʵ����淴Ӧʱ��仯��������ͼ����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

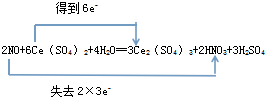 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ka1 | Ka2 | |
| H2A | 1.3��10-2 | 6.3��10-6 |
| H2B | 4.2��10-7 | 5.6��10-7 |
| A�� | H2A�ĵ��뷽��ʽ��H2A�T2H++A2- | |
| B�� | �����£���ˮ��Na2B��ˮ��ƽ�ⳣ��Ϊ��Ka1=$\frac{K_W}{{4.2��{{10}^{-7}}}}$ | |
| C�� | ��Ũ�ȵ�Na2A��Na2B��Һ����ˮ���������H+Ũ�ȴ�С��ϵΪ��ǰ�ߴ��ں��� | |
| D�� | ��Na2B��Һ�м�������H2A��Һ���ɷ�����Ӧ��B2-+H2A=A2-+H2B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������������Fe��OH��3+3H+�TFe3++3H2O | |
| B�� | AlƬ������NaOH��Һ��Ӧ���������壺2Al+2OH-+2H2O�T2Al��OH��3+3H2�� | |
| C�� | ��̼�������Һ�мӹ���ʯ��ˮ�����ȣ�NH4++OH-�TNH3•H2O | |
| D�� | ���ữ�ĸ��������Һ����˫��ˮ��2MnO4-+6H++5H2O�T2Mn2++5O2��+8H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ۢܢ� | C�� | �ۢ� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com