
【题目】下列各组离子中,在酸性溶液中能大量共存,且溶液为无色透明的是( )
A.K +、.MnO 4﹣、Cl ﹣、SO 42﹣
B.Na +、CO 32﹣、Cl ﹣、SO 42﹣
C.NO 3﹣、Na +、HCO 3﹣、Ba 2+
D.Na +、NO 3﹣、NH 4+、SO 42﹣
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】常温下,向H2C2O4溶液中逐滴滴加NaOH溶液,若定义pc=-lgc,则所得溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)与溶液pH的关系如图所示。下列说法正确的是

A. 常溫下,Ka1(H2C2O4)=10-1.3
B. pH=x时,c(HC2O4-)<c(H2C2O4)=c(C2O42-)
C. M点时,c(Na+)<2c(HC2O4-)+c(C2O42-)
D. ![]() 随pH的升高而增大
随pH的升高而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V mL硫酸铝溶液中含Al3+a g,取V/4 mL溶液稀释到4V mL,稀释后溶液中SO42-的物质的量浓度是
A. 125a/9V mol/L B. 125a/18V mol/L
C. 125a/36V mol/L D. 125a/54V mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是

A. 4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
B. 2Na+Cl2![]() 2NaCl
2NaCl
C. Zn+CuSO4===ZnSO4+Cu
D. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
(1)还原剂是________,还原产物__________。
(2)浓硝酸在反应中表现出来的性质是________________。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(3)当有9.6g铜参与反应时,在标准状况下,产生气体的体积为________,转移的电子数为___________。
(4)用双线桥法标出电子转移的方向和数目______。
Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验需用0.4molL﹣1 NaOH溶液480mL.配制方法如下:
(1)配制该溶液所需的仪器有:量筒、天平、药匙、烧杯、玻璃棒、___、_____;
(2)用托盘天平准确称量___________g 固体NaOH;
(3)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是_________,对实验结果没有影响的是_____________(填各选项的序号).
A.所用的NaOH中混有少量Na2O
B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,仰视容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是有机化工原料和优质燃料,主要应用于精细化工、塑料等领域,也是农药、医药的重要原料之一。
(1)已知反应CO(g)+2H2(g)== CH3OH(g) H= —99kJ.mol—1中的相关化学键键能如下:
化学键 | H-H | C-O | C≡O | H-O | C-H |
E/(kJ.mol-1) | 436 | 343 | x | 465 | 413 |
则x=___________________。
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)![]() CH3OH(g) ,
CH3OH(g) ,
CO在不同温度下的平衡转化率(α)与压强的关系如图所示。
①a、b两点的反应速率:v(b)____v(a)(填“>”、“<”或“=”)。②该反应的△S______0,图中的T1______T2(填“>”、“<”或“=”)。
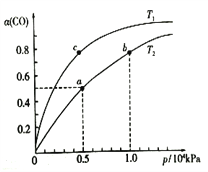
③该合成反应的温度一般控制在240~270℃,选择此温度范围的原因是:
I.此温度范围下的催化剂活性高;
II.______________________________________________________。
④图中a点的压强平衡常数KP=_______________(KPa)-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)利用合成气(主要成分为CO和H2)合成甲醇,发生主要反应如下:
I:CO(g)+2H2(g)![]() CH3OH(g) H1
CH3OH(g) H1
II:CO2(g)+H2(g) ![]() CO(g) + H2O(g) H2
CO(g) + H2O(g) H2
III:CO2(g)+3H2(g)![]() CH3OH(g) + H2O(g) H3
CH3OH(g) + H2O(g) H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如下图所示。
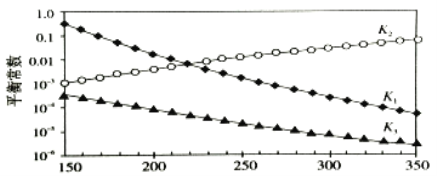
则H1___________H3(填“>”、“<”或“=”), 理由是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A. 无色透明的溶液中:Fe3+、NH、I—、CO![]()
B. 0.1 mol·L-1 KNO3溶液中:Na+、Fe2+、Cl—、SO![]()
C. 使甲基橙变红的溶液中:Na+、Mg2+、SO![]() 、AlO
、AlO
D. 水电离产生的c(H+) =10-13mol·L-1的溶液中:K+、Ca2+、NO、HCO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com