
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1 盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),
(3)他们记录的实验数据如下:
已知:Q=Cm(t2 -t1 ),反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均为1g·cm-3。
),反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均为1g·cm-3。
实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
t1 | t2 | ||||
① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
根据实验数据计算并写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响。
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源:2016-2017学年湖北省高二上学期期中化学试卷(解析版) 题型:实验题
(1)50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH 溶液在如图所示的装置中进行中和反应。通过测定反应过程中 所放出的热量可计 算中和热。回答下列问题:
算中和热。回答下列问题:
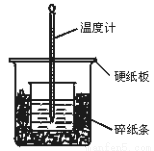
①从实验装置上看,图中尚缺少的一种玻璃用品是__________________。
②实验中改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L NaOH 溶液进行反应,与上述实验相比,所求的中和热_________(填“相等”或“不相等”)。
(2)①如图Ⅰ 表示10 mL量筒中液面的位置。A与B,B与C刻度间相差1 mL,如果刻度A为6,量筒中液体的体积是________mL。
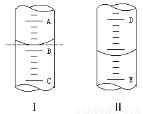
②图Ⅱ表示50 mL滴定管中液面的位置。如果液面处的读数是a,则滴定管中液体的体积(填代号)________。
A.是a mL B.一定大于a mL
C.是(50-a) mL D.一定大于(50-a) mL
(3)已知KMnO4、MnO2在酸性条件下均能将草酸 (H2C2 O4)氧化:
O4)氧化:
(i)MnO4-+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)
(ii)MnO2+H2C2O4+2H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入1.80g草酸,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.020mol·L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。试回答下列问题:
① 方程式(i)配平后H2C2O4的计量系数为 。
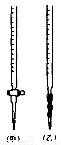
② 0.020mol·L-1KMnO4标准溶液应置于 (填“甲”或“乙”)滴定管中;滴定终点的颜色变化是 。
③ 你能否帮助该研究小组求得软锰矿中MnO2的质量分数;若“能”,请给出计算结果;若“否”,试说明原因。“能”的计算结果或“否”的原因说明 。
④若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
A.滴定前尖嘴部分有一气泡,滴定终点时消失
B.溶液转移至容量瓶中,未将烧杯、玻棒洗涤
C.滴定前仰视读数,滴定后俯视读数
D.定容时,俯视刻度线
E.锥形瓶水洗之后未用待测液润洗
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期第一次月考化学试卷(解析版) 题型:填空题
O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为____________,原子个数比为____________。
(2)等温等压下,等体积的O2和O3所含分子个数比为____________,原子个数比为____________,质量比为_________。
(3)配制100 mL 1 mol·L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为1.84 g·mL-1,质量分数为98%)的体积为____________mL。
(4)现要配制1 mol·L-1 Na2CO3溶液250 mL,求:①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)_____ _______ g;②需要物质的量浓度为4 mol·L-1的Na2CO3溶液____________ mL;
mL,求:①需要含结晶水的碳酸钠晶体(Na2CO3·10H2O)_____ _______ g;②需要物质的量浓度为4 mol·L-1的Na2CO3溶液____________ mL;
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期第一次月考化学试卷(解析版) 题型:选择题
4 ℃时,若20滴水恰好为1 mL,那么1滴水中所含的水分子数约为(NA表示阿伏加德罗常数的值)( )
A.20NA B.NA/360
C.9NA/10 D.360/NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列实验目的能够实现的是( )
A. 用托盘天平称取3.23 g NaCl固体 B. 用50 mL量筒量取30.12 mL水
C. 向小试管中加入100 mL稀盐酸 D. 用胶头滴管取约1 mL溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:选择题
对下列实验的描述不正确的是( )

A.图(a)所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性
B.图(b)所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀
C.图(c)所示的实验:根据温度计读数的变化用稀盐酸和稀N aOH溶液反应测定中和热
aOH溶液反应测定中和热
D.图(d )所示的实验:根据两烧瓶中气体颜色的变化判断2NO2(g)
)所示的实验:根据两烧瓶中气体颜色的变化判断2NO2(g) N2O4(g)是放热反应
N2O4(g)是放热反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.对于有气体参与的反应,增大压强,活化分子总数增多,化学反应速率增大
B.对放热反应而言,升高温度,活化分子百分数减少,化学反应速率减小
C.活化分子间发生的碰撞为有效碰撞
D.使用催化剂,活化分子百分数增多,化学反应速率增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上期中化学试卷(解析版) 题型:选择题
已知100℃时,水的离子常数积为1×10-12。100℃时0.1mol·L-1的HX溶液中,c (OH-)/c (H+) =1×10-6,在该条件下对0.1mol·L-1的HX溶液,下列说法中正确的是
A.HX的电离方程式为:HX=H+ + X-
B.此溶液的pH=1
C.该溶液中c(HX)> c (H+)> c (X-)>c (OH-)
D.NaX与HX的混合溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:填空题
在25℃时,pH = 12的NaOH溶液100 mL ,欲使它的pH降为11,需加入pH = 10的NaOH溶液___________ mL ;在25℃时,有pH为a的盐酸和pH为b的NaOH溶液等体积混合:若a+b=13,则溶液呈 性;pH为2的盐 酸和pH为12的NaOH溶液,由水电离的氢离子浓度之比为 。
酸和pH为12的NaOH溶液,由水电离的氢离子浓度之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com