
 CO2↑+2SO2↑+2H2O
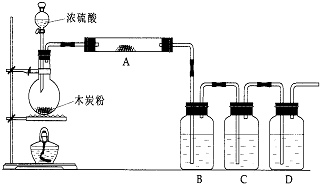
CO2↑+2SO2↑+2H2O分析 (1)用微热法检验装置的气密性,注意从“微热、密闭、气泡、水柱”四点答题;
(2)浓硫酸和碳在加热条件下反应生成二氧化碳、二氧化硫和水,正确书写化学反应方程式;
(3)验证生成产物成二氧化碳、二氧化硫和水,需要先利A用无水硫酸铜检验水蒸气的生成,依次用B检验二氧化硫气体用品红试液褪色证明,C装置利用高锰酸钾溶液除去二氧化硫,D装置中利用澄清石灰水变浑浊证明二氧化碳的存在;
(4)C装置利用足量高锰酸钾溶液除去二氧化硫,正确描述现象.
解答 解:(1)用微热法检验装置的气密性,注意从“微热、密闭、气泡、水柱”四点,可在反应前先在B、C、D中加水,关闭分液漏斗的活塞.再点燃酒精灯,加热烧瓶一小会儿.在瓶D中出现气泡,熄灭酒精灯,瓶B、C、D中导管液面上升,形成一段水柱,证明该装置不漏气,
故答案为:反应前先在B、C、D中加水,关闭分液漏斗的活塞.再点燃酒精灯,加热烧瓶一小会儿,在瓶D中出现气泡,熄灭酒精灯,瓶B、C、D中导管液面上升,形成一段水柱,证明该装置不漏气.
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:2H2SO4(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
故答案为:2H2SO4(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(3)A.加入的试剂是无水硫酸铜,作用是检验水;
B.加入的试剂是品红溶液,作用是检验二氧化硫;
C.加入的试剂是足量酸性KMnO4 溶液,作用是除去SO2;
D.加入的试剂是澄清石灰水,作用是检验CO2;
故答案为:足量酸性KMnO4 溶液; SO2;
(4)用B检验二氧化硫气体用品红试液褪色证明,C装置利用高锰酸钾溶液除去二氧化硫,D装置中利用澄清石灰水变浑浊证明二氧化碳的存在,但是二氧化硫也可以使澄清石灰水变浑浊,为了不干扰二氧化碳的检验,C装置中的高锰酸钾要足量,故现象为:导管有气泡冒出,溶液紫色逐渐变浅或紫色不退尽.
故答案为:导管有气泡冒出,溶液紫色逐渐变浅或紫色不退尽.
点评 本题考查性质实验设计,侧重于学生的分析能力、实验能力的考查,注意在解实验探究题时,首先要了解实验目的,认真分析题中反应原理,然后结合所给信息和学过的知识分析解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 苯酚钠溶液 | B. | 碳酸氢钠溶液 | C. | 碳酸钠溶液 | D. | 醋酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广燃煤脱硫技术,减少SO2污染,同时把煤粉碎了再燃烧以提高煤的燃烧效率 | |
| B. | 开发新能源,如太阳能、风能等,减少对化石能源的依赖 | |
| C. | 在汽车尾气处理器中使用新的催化剂,促使汽车尾气中CO和NO转化为无污染物 | |
| D. | 化石燃料燃烧产生的CO2、SO2、NO2都会导致酸雨的形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏的方法来分离甲苯、溴苯和辛烷的混合物 | |
| B. | 催化裂化不仅可以提高汽油的产量而且可以提高汽油质量 | |
| C. | 裂化汽油可使溴水褪色 | |
| D. | 裂解的目的是获得乙烯、丙烯、丁二烯等短链不饱和烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚丙烯的结构简式为: | B. | 氯化氢的电子式为: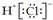 | ||
| C. | 甲烷的比例模型: | D. | 质量数为35的氯原子:${\;}_{35}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑧ | ⑩ | |||
| 3 | ① | ⑦ | ⑨ | |||||
| 4 | ② | ③ |
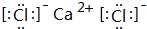 ,化学键类型为离子键(“离子键”或“共价键”).
,化学键类型为离子键(“离子键”或“共价键”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物中酯A的相对分子质量为88 | |
| B. | 18O全部进入水中 | |
| C. | 18O全部进入生成的酯中 | |
| D. | 酯A与H2O水解后在CH3COOH和CH3CH2OH都有18O存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com