
| 4 |
| 3 |
| 1 |
| 3 |
| 4 |
| 3 |
| 1 |
| 3 |


科目:高中化学 来源: 题型:
A、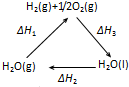 △H1=△H2+△H3 |
B、 在催化剂条件下,反应的活化能等于E1+E2 |
C、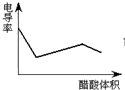 表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 |
D、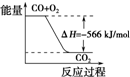 可表示由CO(g)生成CO2(g)的反应过程和能量关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 | 150 | 200 |
| 溶解度(g/100gH2O) | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.11 | 0.092 | 0.074 | 0.034 | 0.012 |
| A、氢氧化钙的溶解是放热过程 |
| B、100℃时氢氧化钙的Kxp约等于4×10-6 |
| C、温度升高时氢氧化钙溶解速率加快 |
| D、100℃时pH=12的溶液中c(Ca2+)≤0.04mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
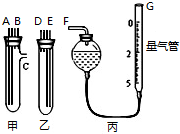 某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案:
某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案: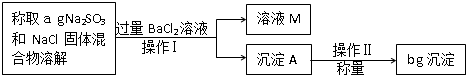
查看答案和解析>>
科目:高中化学 来源: 题型:
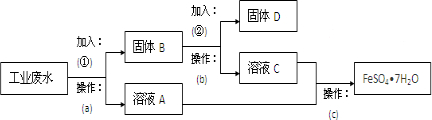
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(Cl-)>c(OH-)>c(H+) |
| B、c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C、c(Na+)=c(Cl-)>c(H+)>c(OH-) |
| D、c(Cl-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com