
| A、MnO4- |
| B、CH3COO- |
| C、S2O32- |
| D、Br- |
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 4.0 |
| A、向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度 |
| B、四种溶液中,水的电离程度最大的是NaClO |
| C、常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3 |
| D、NaHSO3溶液中离子浓度大小顺序为c(Na+)>c(H+)>c(HSO3-)>c(SO32-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/℃ | 200 | 300 | 400 |
| H2的体积分数 | a1 | a2 | 25% |
| A、a1<a2 |
| B、若反应在400℃下进行,则达到平衡时N2的转化率为20% |
| C、若反应在300℃下进行,则达到平衡时反应放出的热量为23.1 kJ |
| D、若反应在200℃下进行,则达到平衡时N2的体积分数为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
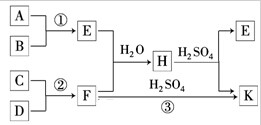
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH3?H2O |
| B、NaOH |
| C、NiO |
| D、CaCO3浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有AgCl沉淀生成 |
| B、无AgCl沉淀生成 |
| C、有沉淀生成但不是AgCl |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学受2Mg+CO2
某同学受2Mg+CO2
| ||
| 实验操作 | 预期现象 | 结论 |
| (1)取少许反应后试管C中的溶液,加入足量的BaCl2溶液 | 无白色沉淀产生 | 证明假设 |
| (2)若有白色沉淀产生,再检测(1)的上层溶液的PH | 若PH>7 | 则溶液中溶质是 |
| 若PH=7 | 则溶液中溶质是 | |
| 若PH<7 | 则溶液中溶质是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com