
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 1.3 | 3.3 | 7.5 | 10.3 |
| 完全沉淀 | 2.8 | 5.2 | 9.7 | 12.2 |


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
| A、常温、常压下,16 g O3中含有的氧原子数为NA |
| B、7.8 g Na2O2与水充分反应,转移的电子数为0.2 NA |
| C、0.1 mol Fe与0.1 mol Cl2充分反应,转移的电子数为0.3NA |
| D、标准状况下,11.2 L H2O中含有的氢原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当Y是金属时,X可能是金属,也可能是非金属 |
| B、当X、Y都是非金属时,Y的非金属性一定比X强 |
| C、当X、Y都是金属时,Y的金属性一定比X强 |
| D、当Y是非金属时,X可能是金属也可能是非金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图装置,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.查看答案和解析>>
科目:高中化学 来源: 题型:
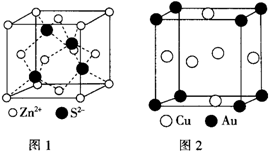 1967年舒尔滋提出金属互化物的概念,其定义为固相金属间化合物拥有两种或两种以上的金属元素,如Cu9Al4、Cu5Zn8等.回答下列问题:
1967年舒尔滋提出金属互化物的概念,其定义为固相金属间化合物拥有两种或两种以上的金属元素,如Cu9Al4、Cu5Zn8等.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱电解质 | 电离平衡常数(Ka或 Kb) |
| CH3COOH | 1.8×10-5 |
| NH3?H2O | 1.8×10-5 |
| 难溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1.1×10-10 |
| BaCO3 | 2.6×10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
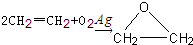
查看答案和解析>>
科目:高中化学 来源: 题型:
| OH- | CO | Cl- | NO | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 不 | 溶 | 溶 |
| Ba2+ | 溶 | 不 | 溶 | 溶 |
| Mg2+ | 不 | 微 | 溶 | 溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com