
【题目】阿伏加德罗常数的值为NA。下列说法正确的是( )
A.1mol乙醇所含共价键数目为6NA
B.22.4LC2H4和C2H6混合气体含有的碳原子数是2NA
C.18g葡萄糖分子中含羟基数目为0.6NA
D.标准状况下,6g乙酸和丙醇(C3H8O)的混合物中含有的分子数为0.1NA
科目:高中化学 来源: 题型:
【题目】如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图;装置(Ⅰ)的离子交换膜只允许Na+通过。电池充、放电的化学方程式为2Na2S2+NaBr3![]() Na2S4+3NaBr。当闭合K时,X极附近溶液先变红色。下列说法正确的是( )
Na2S4+3NaBr。当闭合K时,X极附近溶液先变红色。下列说法正确的是( )
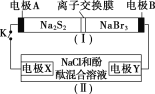
A.装置(Ⅰ)中Na+从右到左通过离子交换膜
B.电极A的电极反应式为NaBr3+2Na++2e-=3NaBr
C.电极X的电极反应式为2Cl--2e-=Cl2↑
D.每有0.1molNa+通过离子交换膜,电极X上就析出标准状况下的气体1.12L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均釆用虚线表示。
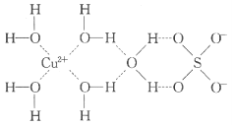
(1)写出基态Cu原子的核外电子排布式____,S原子的价层电子排布图______
(2)写出胆矾晶体中水合铜离子的结构简式_____(必须将配位键表示出来)。
(3)向CuSO4溶液中滴加氨水,可以得到深蓝色的溶液,再加入乙醇后析出深蓝色晶体,写出深蓝色晶体的化学式_____。比较NH3和[Cu(NH3)4]2+中H-N-H 中键角的大小:NH3_____[Cu(NH3)4]2+(填“![]() ” “
” “![]() ” 或“=”)。
” 或“=”)。
(4)已知H2O2的结构如图:
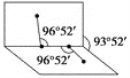
H2O2分子不是直线形的,两个H原子犹如在半展开的书的两面纸上,书页角为93°52′,而两个O—H键与O—O键的夹角均为96°52′,估计它难溶于CS2,简要说明原因______。
(5)分析下表中两种物质的键能数据(单位:kJ/mol)。
A—B | A=B |
| |
CO | 357.7 | 798.9 | 1 071.9 |
N2 | 154.8 | 418.4 | 941.7 |
结合数据说明CO比N2活泼的原因:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是( )
A.Na与O2B.Na2O2与CO2C.NaOH与CO2D.Cu与HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是
A. 乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH→CH3COO+CH3CH2O+H2O
B. 醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2→Cu2++2H2O
C. 苯酚钠溶液中通入少量二氧化碳:2![]() +CO2+H2O
+CO2+H2O![]() 2
2![]() +CO
+CO![]()
D. 乙醛溶液与新制氢氧化铜碱性悬浊液共热CH3CHO+2Cu(OH)2+OH![]() CH3COO+ Cu2O↓+3H2O
CH3COO+ Cu2O↓+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

已知:①RCHO+CH3CHO ![]() RCH=CHCHO+H2O;②
RCH=CHCHO+H2O;②![]() 。
。
回答下列问题:
(1)C的结构简式为_______________________。
(2)F中官能团的名称为___________________。
(3)B与新制Cu(OH)2悬浊液反应的化学方程式为________________。
(4)从转化流程图可见,由D到E分两步进行,其中第一步反应的类型为__________。
(5)化合物G的二氯代物有__________种同分异构体。
(6)芳香化合物X是D的同分异构体,X能发生银镜反应,其核磁共振氢谱显示有3种化学环境的氢,峰面积之比为6∶1∶1,符合条件的X的结构共有多种,任写出2种符合要求的X的结构简式________、___________。
(7)写出用甲醛和乙醛为原料制备化合物CH2=CHCOOCH3的合成路线(其他试剂任选)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中有丰富的矿产、能源、药物、水产等化学化工资源,下图是某工厂对海水资源综合利用的示意图。下列有关说法正确的是 ( )
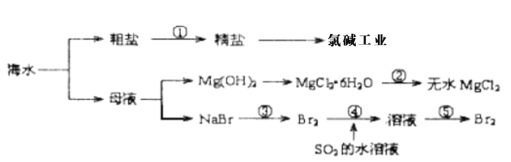
A.海水中含有丰富的Mg元素,利用母液沉淀Mg2+时,使用是石灰乳作为沉淀剂
B.流程②为:将MgCl2·6H2O在空气中受热分解即可制的无水MgCl2
C.在流程③④⑤中溴元素均被氧化
D.流程①中欲除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,操作步骤为:依次加入BaCl2溶液、NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据统计城市机动车辆每年以15%至20%的速度增长,交通事故也频发,汽车在剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。则下列判断正确的是
A. 还原剂与氧化产物的物质的量之比为5:8
B. 若氧化产物比还原产物多1.4mol则转移电子为1mol
C. 每生成1.6mol氮气,则有0.2molKNO3被氧化
D. NaN3是只含有离子键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有氧化还原反应:3H2O2 + 2H2CrO4 =2Cr(OH)3 + 3O2 ↑+ 2H2O
①用单线桥标出反应中的电子转移数目和方向_____________;
②其中Cr被___________,H2O2作___________剂;
③反应转移了0.3mol电子,则产生的气体在标准状态下体积约为__________。
(2)①将用砂纸打磨过的铝片用坩埚钳夹住在酒精灯上点燃,现象是:________;
②在试管中加入少量Na2O2再加入少量水,用带火星的木条伸入试管,再滴入几滴酚酞,可观察到的现象是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com