
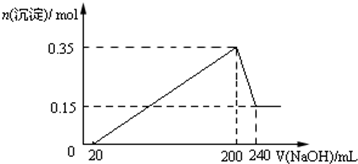
| n |
| v |
| 0.2mol |
| 0.04L |
| 0.15��2+0.2��3 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������͵���-KI��ֽ��������е�KIO3��IO3-+5I-+6H+=3I2+3H2O |
| B��CO��g����ȼ������283.0kJ?mol-1����2CO2��g��=2CO��g��+O2��g����Ӧ�ġ�H=-566.0kJ?mol-1 |
| C��Fe��OH��3��������Fe��OH��3+3H+=Fe3++3H2O |
| D����ij������Һ�к��е����ʵ�����Cl-��AlO2-��CO32-��NO3-��SiO32-��I-�������֣����������������������ݣ���Һ��ɫ�����������������3�֣���ԭ��Һ��һ����CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��27% | B��28% |
| C��54% | D�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾΪ���������IJ��ֽṹ��
��ͼ��ʾΪ���������IJ��ֽṹ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���٢ۢ� |
| C���ڢܢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��m��n��Q��0 |
| B��m��n+P��Q��0 |
| C��m��n��Q��0 |
| D��m��n+P��Q��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A��NaAlH4�к������Ӽ��ͷǼ��Թ��ۼ� |
| B��ÿ����11.2 L����״���£�H2��ת��NA������ |
| C��NaAlH4����Ԫ��Ϊ+1�ۣ��ڷ�Ӧ����50%���ⱻ��ԭ |
| D����Ӧ�����������뻹ԭ��������ʵ���֮��Ϊ1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������--Fe2O3--���� |
| B������--CuSO4?5H2O--������Һ |
| C������ʯ--SiO2--��Ʒ |
| D������--NaHCO3--���Ƹ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
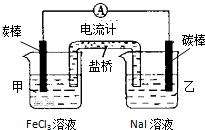
| A����Ӧ��ʼʱ������ʯī�缫�Ϸ���������Ӧ |
| B����Ӧ��ʼʱ������ʯī�缫��Fe3+����ԭ |
| C�������ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬ |
| D�������ƶ���Ϊ����ڼ�������FeCl2���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com